Sono un ricercatore, impegnato da più di dieci anni in progetti di immunologia dei tumori e terapia genica. Nel momento in cui credo di avere raggiunto un risultato di rilievo, il mio primo pensiero è di sottoporlo al vaglio della comunità scientifica (la cosiddetta “revisione tra pari”, in inglese “peer-review”) per vedere se la mia indagine sperimentale e le mie conclusioni stanno in piedi. Se la mia ricerca supera questo controllo, viene resa pubblica.
Davide Vannoni non ha, fino ad oggi, mostrato alla comunità scientifica risultati sperimentali su Stamina, per cui sono rimasto piacevolmente sorpreso dalla recente pubblicazione sulla sua pagina Facebook di alcune diapositive che costituiscono la prima –seppur parziale- condivisione di dati scientifici relativi a Stamina.
Ho ritenuto opportuno e rilevante commentare questi dati, per quanto possibile, da un punto di vista divulgativo ma scientifico, e auspico che numerosi altri colleghi facciano lo stesso al fine di surrogare quella “revisione tra pari” fino ad oggi evitata.
PRIMA DIAPOSITIVA – VITALITÀ DELLE CELLULE SCONGELATE
Obiettivi dell’esperimento: valutare la vitalità e il numero delle cellule che poi verosimilmente saranno infuse a un ammalato.
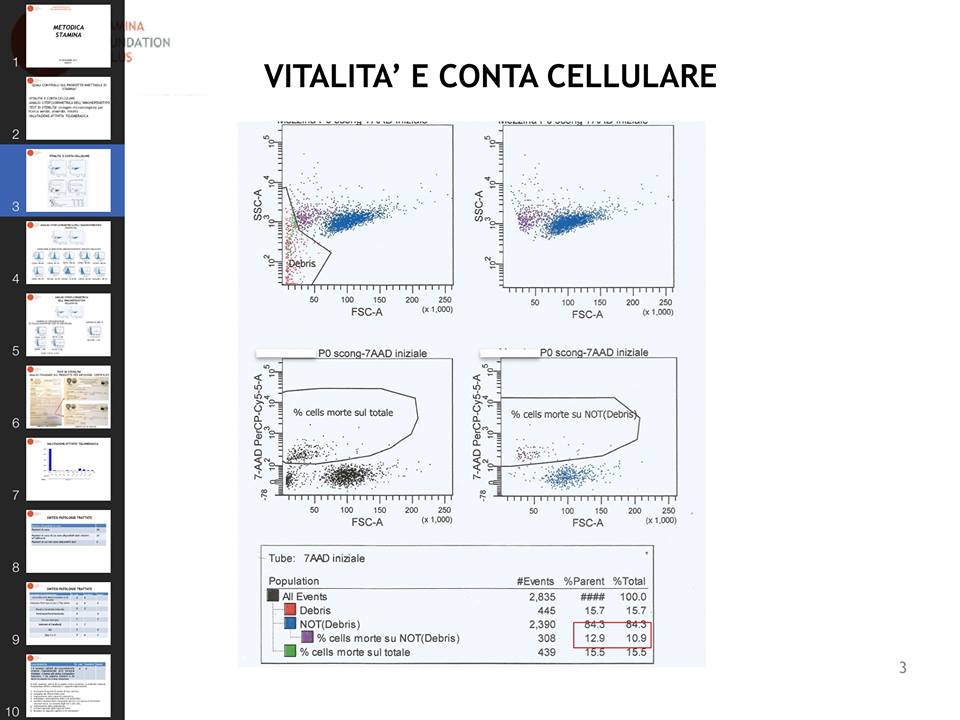
Come è stato condotto: le cellule, presumibilmente ottenute tramite metodica Stamina e congelate, sono state scongelate e colorate con 7AAD, un colorante che marca il DNA delle cellule morte.
L’esperimento è stato quindi analizzato tramite citofluorimetria a flusso. Il grafico in alto a sinistra riporta la dimensione delle cellule (parametro FSC, asse X) in relazione alla loro granulosità (parametro SSC, asse Y). Ogni puntino è una cellula. Si nota immediatamente una popolazione di detriti cellulari molto piccoli e scarsamente granulari, che sono “avanzi” di cellule morte (in linguaggio tecnico “debris”). Questi sono stati circondati da un “gate” elettronico (la linea denominata “debris”) ed eliminati dal grafico successivo in alto a destra. Il grafico in basso a destra rappresenta la dimensione delle cellule (asse X) in relazione alla loro colorazione con 7AAD (asse Y). Le cellule morte vengono definite come cellule piccole e positive per 7AAD (gate “% cellule morte su NOT debris”), e ne viene calcolata la percentuale rispetto all’intera popolazione cellulare.
Cosa ci dice: Escludendo i debris (inerti), in questa preparazione c’è il 12,9% di cellule morte e l’87,1% di cellule vive e quindi potenzialmente attive.
Cosa non ci dice: L’esperimento non ci dice quante cellule in totale ci sono nel campione analizzato, né sul parametro cruciale di quante cellule vive siano state somministrate al paziente.
SECONDA DIAPOSITIVA: IMMUNOFENOTIPO DELLE CELLULE

Obiettivi dell’esperimento: L’esperimento si propone di descrivere l’aspetto (“immunofenotipo”) delle cellule tramite la misurazione dell’espressione di alcune molecole caratteristiche (“marcatori”) delle cellule staminali mesenchimali.
Come è stato condotto: Si tratta ancora di un esperimento di citofluorimetria. Le cellule sono state colorate con anticorpi che riconoscono specificamente ciascuna molecola da misurare. Ogni anticorpo è legato a un colorante fluorescente. La macchina misura l’intensità di fluorescenza su ciascuna cellula, che è tanto maggiore quanto la molecola è più espressa.
L’analisi si deve eseguire sulle sole cellule vive, che sono state plausibilmente definite soltanto come cellule “grandi” (grafici in alto, asse X, FSC elevato). Si nota che l’analisi con 7AAD non può essere stata eseguita perché interferirebbe con alcune analisi successive, e non è riportato se sia stata sostituita con metodiche equivalenti.
I dieci istogrammi in basso si leggono solo guardando l’asse X. Maggiore è il segnale sull’asse X, maggiore l’espressione della molecola annotata sotto al grafico. L’istogramma in basso a sinistra riporta un’etichetta sbagliata (CD29 invece di CD166).
Seppure su ogni istogramma sia stato indicato il confine tra un campione negativo e uno positivo (attraverso i gate indicati dalla lettera “P” e un numero), esso può essere stato disegnato in modo assolutamente arbitrario dall’esecutore dell’esperimento. Per questa ragione, il segnale di fluorescenza deve essere sempre confrontato con un adeguato controllo negativo, che in questo caso non è né descritto né mostrato.
Cosa ci dice: Qualora la distinzione tra campione positivo e negativo fosse stata operata correttamente, l’esperimento indicherebbe che, per questo paziente, le cellule prodotte con metodo Stamina hanno un aspetto che per alcuni tratti coincide con quello delle cellule staminali mesenchimali.
Cosa non ci dice: L’esperimento si concentra sull’aspetto delle cellule di un solo paziente, che potrebbe non rappresentare ciò che viene ottenuto “di routine” con il metodo Stamina. Infatti, la diapositiva numero 4 (vedi oltre) riporta che quasi tutti questi marcatori sono espressi solo debolmente in un paziente evidentemente diverso.
Inoltre, l’esperimento non ci dice se le cellule staminali mesenchimali funzionano correttamente. In particolare, non viene mostrato il dato cruciale e controverso che suggerirebbe che le cellule sono in grado di diventare neuroni.
TERZA DIAPOSITIVA – ESCLUSIONE DELLA TRASFORMAZIONE IN CANCRO

Obiettivi dell’esperimento: L’esperimento si propone di escludere la trasformazione tumorale delle cellule trattate con metodo Stamina tramite la misurazione dell’attività dell’enzima telomerasi. Un’elevata attività telomerasica è infatti caratteristica delle cellule cancerose.
Come è stato condotto: Il grafico mostra l’attività telomerasica delle cellule derivate da 10 pazienti e confrontate in percentuale con una linea cellulare tumorale (K562, prima barra). Esistono diverse metodiche per determinare l’attività della telomerasi (vedi Zhou e Xing, Chem Soc Rev 2012), ma quella utilizzata per produrre questi dati non è indicata.
Cosa ci dice: Per l’interpretazione dell’esperimento, è cruciale sapere se l’attività telomerasica è stata misurata sull’intera popolazione cellulare o sulle singole cellule. Dalla costruzione del grafico si potrebbe desumere che la misurazione sia stata compiuta sull’intera popolazione cellulare. In questo caso, si conclude che le cellule trattate con metodo Stamina hanno IN MEDIA una bassa attività telomerasica, in confronto con la linea tumorale K562.
Cosa non ci dice: In assenza di un test condotto su un campione rappresentativo di singole cellule, non si può escludere che una piccola frazione delle cellule abbia un’attività telomerasica alta, e quindi proprietà tumorali. Si dovrebbe inoltre aggiungere altri test in vitro (valutare il cariotipo, o comuni traslocazioni cromosomiche) per escludere che le cellule abbiano assunto altre caratteristiche proprie delle cellule tumorali. Sarebbe ancora più predittivo inoculare le cellule in vivo per seguire nel tempo l’eventuale insorgenza di tumori. Tali esperimenti sono particolarmente importanti perché è stato descritto che le cellule staminali mesenchimali coltivate in vitro possono dare origine a tumori (Charbord, Human Gene Therapy 2010).
QUARTA DIAPOSITIVA: ANALISI DI STERILITÀ

Obiettivi dell’esperimento: I test di sterilità sono volti a escludere che le cellule trattate con metodo Stamina siano contaminate da agenti biologici estranei che potrebbero causare patologie nel paziente.
Come è stato condotto: La presenza di batteri e funghi viene attestata coltivando in vitro un piccolo campione del tessuto da testare in condizioni che favoriscono lo sviluppo di funghi e batteri. Se non si osserva alcuna crescita di microorganismi, si esclude la contaminazione.
Si nota che la diapositiva è mal costruita: la parte sinistra e quella destra si riferiscono a pazienti diversi. Inoltre la parte destra sembra riferirsi a un test generale su campione di midollo osseo più che a cellule staminali mesenchimali prodotte con metodo Stamina.
Cosa ci dice: Questi test escludono la presenza di contaminazione da funghi o batteri.
Cosa non ci dice: Il risultato è parziale. Per somministrare un prodotto sicuro a un paziente è assolutamente necessario escludere contaminazioni da molti altri agenti patogeni come batteri intracellulari (micoplasma) e virus (HIV, epatite C).
CONCLUSIONI:
La diapositiva uno dimostra una buona vitalità delle cellule infuse.
I risultati dell’immunofenotipo sono incoerenti: la diapositiva due presenta un caso in cui la maggioranza dei marcatori caratteristici delle cellule mesenchimali sono molto espressi, la diapositiva quattro presenta un altro caso, dove tali marcatori sono scarsamente espressi.
Il saggio di attività telomerasica non è sufficiente, di per sé, a escludere la trasformazione tumorale di parte delle cellule mesenchimali.
Le indagini di sterilità sono presentate in modo incompleto.
I dati disponibili sono quindi frammentari, e vengono taciuti particolari essenziali quali il numero di cellule infuse per ogni paziente, se (ed in quale percentuale) queste cellule sono in grado di diventare neuroni, ed una valutazione clinica precisa dei pazienti. Tali dati sono a tutt’oggi indisponibili.
[Francesco Marangoni]
Francesco Marangoni è Ricercatore al Massachusetts General Hospital e alla Harvard Medical School di Boston. In 12 anni di attività scientifica ha ricevuto 13 riconoscimenti e pubblicato 14 articoli in riviste peer-reviewed tra cui The Journal of Experimental Medicine, Immunity e Nature. È revisore per il Ministero della Sanità (Bando Ricerca Finalizzata 2011-2012) ed ha collaborato alla revisione scientifica di numerosi articoli su riviste ad alto impact factor tra cui Nature e Science.
GLOSSARIO
7AAD: un colorante fluorescente del DNA che può entrare solo nelle cellule morte. È comunemente usato per escludere le cellule morte dall’analisi citofluorimetrica.
Campione negativo: Un campione sperimentale che non esprime una determinata caratteristica.
Campione positivo: Un campione sperimentale che esprime una determinata caratteristica.
Cariotipo: È la caratterizzazione morfologica dei cromosomi di una cellula. Nell’uomo, il cariotipo normale è costituito da 22 coppie di cromosomi e 2 cromosomi sessuali, ognuno dei quali caratterizzato da una specifica forma e dimensione. In presenza di gravi lesioni genetiche, il cariotipo appare alterato.
CD: È una sigla utilizzata nella nomenclatura delle molecole. La specifica molecola viene indicata dal prefisso CD, un numero progressivo, ed una lettera (facoltativa, presente solo se sussistono ambiguità). Esempio: esistono varie molecole chiamate CD1, una delle quali è CD1a.
Cellule staminali mesenchimali: sono cellule non completamente specializzate, in grado di diventare cellule ossee, cartilaginee, e adipose. La loro capacità di diventare cellule neuronali è controversa.
Citofluorimetria a flusso: È una tecnica in grado di misurare la grandezza e la fluorescenza di ogni singola cellula. È una tecnica veloce, che permette la misurazione di 2000 – 20000 cellule per secondo. È particolarmente utile per misurare la quantità di una molecola in una cellula: per fare questo si utilizzano anticorpi specifici che legano quella particolare molecola, e sono anche coniugati con un colorante fluorescente. In questo caso, la misura dell’intensità di fluorescenza di una cellula è proporzionale all’espressione della molecola.
Controllo negativo: È un campione che, nonostante sia sottoposto al medesimo trattamento di tutti gli altri campioni sperimentali, dà risultato nullo. È indispensabile per misurare il “rumore di fondo” intrinseco di qualsiasi misurazione.
Debris: Sono frammenti di cellule morte, probabilmente inerti.
FSC: In citofluorimetria, è l’acronimo di “Forward scatter”, e costituisce una misura della dimensione della cellula.
Gate elettronico: In citofluorimetria, è un contorno mono o bidimensionale che seleziona una popolazione di cellule per analisi successive. È anche utile per misurare la percentuale di cellule contenute nel gate.
Immunofenotipo: È l’aspetto delle cellule definito da esperimenti di citofluorimetria.
Linea cellulare: Si tratta di una popolazione di cellule che si può espandere indefinitamente mediante cultura in vitro. Nella maggioranza dei casi, si tratta di cellule tumorali.
Marcatore: In generale, è una molecola espressa in modo caratteristico da una cellula. Specificamente in citofluorimetria, sono le molecole misurate tramite anticorpi specifici coniugati a molecole fluorescenti.
Revisione tra pari: (in inglese “peer-review”) Il processo secondo cui un’indagine scientifica viene approfonditamente rianalizzata da altri ricercatori anonimi, che ne giudicano la qualità e propongono miglioramenti. È il passo obbligato prima di ogni pubblicazione scientifica e ogni richiesta di finanziamento.
SSC: In citofluorimetria, è l’acronimo di “Side scatter”, e costituisce una misura di quanti granuli sono contenuti in una cellula.
Telomerasi: È un enzima che mantiene elevata la lunghezza dei telomeri, elementi del cromosoma che progressivamente si accorciano durante l’invecchiamento delle cellule. Una eccessiva attività della telomerasi è sufficiente per lo sviluppo del tumore.
Traslocazione cromosomica: È una lesione genetica caratterizzata dal distacco di un pezzo di cromosoma, e dalla sua successiva fusione a un altro cromosoma. I geni ibridi che si creano talvolta scompaginano la normale crescita cellulare originando tumori. Sono lesioni comuni nel cancro.








Ottimo lavoro!
Guardi che Vannoni, ha solo voluto rispondere a chi diceva non avesse condotto alcuna valutazione sulle cellule da lui prodotte.
Le sue considerazioni son quindi totalmente fuori luogo.
Quindi un ricercatore della Harvard medical fa un’analisi puramente scientifica, senza nessuna critica personale, ed è FUORI LUOGO????? Siete una setta con il vostro santone Vannoni, con la scienza non avete nulla a che fare.
Nessuna setta, solo logica. E voi non la seguite !
la logica presuppone l’uso di metodiche validate e possibilità di dimostrare risultati ripetibili. Uno scienziato dice “ve lo dimostro” un santone “dovete credermi”, non avete nulla di diverso da Mamma Ebe, il Mago Otelma o Vanna Marchi. Solo in un paese dove la gente crede al malocchio come l’Italia potevate avere successo. Alla gente piace credere a chi promette il miracolo, non a chi ragiona con i piedi per terra. A si le BigPharma mi hanno appena dato i 12 milioni che voleva Vannoni, o li ha già presi?
Mi ripeto, nessuna setta, solo logica. E voi non la seguite !
quando non si hanno argomenti si ripetono frasi fatte, tipico di una setta.
Fuori luogo? Al contrario, assolutamente pertinenti
Effettuare degli esperimenti su quelle cellule non significa direttamente fare delle “valutazioni”. La validazione è tale solo se gli esperimenti sono pertinenti E esaustivi nei confronti delle domande poste (aka sono cellule staminali mesenchimali? possono diventare neuroni? quello che viene somministrato è in qualche modo rischioso per il paziente? etc etc). Quello che mostra questo post è che, sebbene gli esperimenti siano in parte pertinenti (ossia si tratta di esperimenti standard nella validazione di colture cellulari) essi sono ben lontani dall’essere sufficienti. Anzi, alcuni esperimenti cruciali mancano. Senza contare che mancano replicati e analisti statistiche (vedi assenza di grafici con dovute barre di errore e p value). Senza dovute analisi statistiche, i singoli esperimenti hanno valore quasi nullo.
Bene, grazie per la vostra disamina di quanto presentato. In realtà queste immagini che sono tratte da una serie molto ampia e completa svolta su ogni paziente (prima e dopo la cripreservazione e per ogni infusione) da parte del laboratorio Nocivelli degli Spedali Civili di Brescia erano postate per dare una prima risposta al fatto che veniva detto che non producevamo cellule staminali, ma solo detriti di cellule morte (che, come potete vedere, anche dopo lo scongelamento sono il 12% della popolazione totale). Per quanto riguarda gli agenti patogeni virali (Hiv, Epatite B, C e sifilide) questi vengono esclusi attraverso analisi DAT del donatore prima del prelievo. Tutto è migliorabile ed anche se abbiamo predisposto per la valutazione da fare a Miami una più ampia caratterizzazione e soprattutto incrociata su diversi CD (siamo infatti convinti che non si tratti di un solo tipo di cellule staminali, ma di più tipo con funzioni rigenerative differenti) siamo sempre pronti a raccogliere suggerimenti e indicazioni da ricercatori che abbiano voglia di aiutarci in questo cammino (e ovviamente a riconoscerne il contributo). La telomerasi è svolta su tutti i pazienti su intere popolazioni cellulari coltivate parallelamente a quelle da inoculare e fatta continuativamente dopo diversi passaggi (fino a 15 passaggi) per misurarne l’andamento. Quello presentato è ovviamente solo un grafico riassuntivo a titolo esemplificativo. Ovviamente è svolta anche l’analisi per il micoplasma.
Se fosse vero che lei non ha nulla da nascondere perché non presenta tutti i risultati e segue le regole, invece di aizzare la sua setta di accoliti? O forse ha molto da nascondere? Non ricominci con la tiritera delle case farmaceutiche cattive che cospirano, per cortesia, visto che lei ha cercato di vendere il suo magico metodo a chiunque. Ma lei Vannoni cammina anche sulle acque, moltiplica i pani e i pesci o specula solo sul dolore e la disperazione di persone malate? Adesso dirà che sono pagato dalle BigPharma… magari…sono solo nauseato dai chi specula sulla sofferenza come lei.
Visto che non ci sono controlli positivi o negativi in nessuna delle diapositive rintracciabili in rete credo che l’obiezione che non sono state svolte adeguate analisi scientifiche resti valida.
… ?
Apprendo con piacere che Stamina Foundation – contrariamente a quanto sostenuto pubblicamente più volte dal Prof. Andolina – riconosce la potenziale cancerogenicità delle cellule staminali ottenute con il cosiddetto Metodo Stamina. Tant’è che si è preoccupata di eseguire analisi estese, sistematiche ed esaustive, al fine di accertare che ogni singola infusione sia priva di cellule potenzialmente cancerogene.
Questo non può che farmi piacere, anzitutto perché queste analisi permetteranno di archiviare almeno uno dei potenziali rischi legati all’uso di cellule staminali. In secondo luogo perché in questo modo è possibile dimostrare che il cosiddetto Metodo Stamina è in grado di produrre nientemeno che «più tipi [di staminali] con funzioni rigenerative differenti», senza che nessuno di essi acquisisca potenzialità neoplastiche. Una vera e propria rivoluzione nel campo della medicina rigenerativa!
Confido quindi che vorrà prontamente condividere – seppure molto tardivamente – con il resto degli scienziati che si occupano di questa promettente branca della medicina, questi importantissimi risultati.
Confido anche che siano disponibili analoghe indagini sperimentali, egualmente complete ed esaustive, riguardanti gli altri rischi legati ai trattamenti con le cellule staminali (reazioni di rigetto, reazioni autoimmunitarie, trombosi, ecc. ).
Confido, infine, che Stamina Foundation sia altresì in possesso di tutta la documentazione necessaria a comprovare dosaggi e maneggevolezza delle infusioni; parametri indispensabili per stabilire quante cellule iniettare in ogni singolo malato per massimizzare i benefici e minimizzare i rischi.
Resto quindi in impaziente attesa di poter consultare tutta la documentazione relativa alla sicurezza del cosiddetto Metodo Stamina, che sono certo non tarderete a rendere di pubblico dominio.
Perché i malati hanno il diritto di sapere.
c’e’ un rapporto dell’ EMA che definisce cancerogene le embrionali e potenzialmente le IPS,le MSC non vengono enunciate in tale rapporto.
Se ha voglia lo puo’ trovare in rete.
L’idea che le cellule staminali mesenchimali (MSC) non presentino rischio di tumore è una leggenda metropolitana. È sufficiente una rapida occhiata su medline per verificarlo.
Inoltre, nulla sappiamo delle cellule che hanno subito il trattamento col Metodo Stamina, per cui, per garantire la sicurezza dei pazienti, è necessario presupporre che siano a rischio neoplasia, fino a prova contraria.
Prova contraria di cui il presidente di Stamina Foundation ha appena affermato di essere in possesso, e che confido non tarderà a rendere di pubblico dominio, anzitutto per tranquillizzare le decine di malati che hanno già ricevuto almeno un’infusione; e inoltre per dovere di correttezza nei confronti di chi volesse in futuro prendere in considerazione la possibilità di sottoporsi ad esse.
Informare i malati riguardo ai potenziali rischi di una terapia – specie se gravi come quelli segnalati per le staminali – è un preciso dovere deontologico.
sig reality e lei pensa che i medici dell’ospedale bresciano non hanno queste informazioni,oppure pensa che il primo che passa prenda ampollina e siringona e opera l’infusione.
Ciò che gli Spedili Civili avevano o non avevano è un problema che riguarda gli Spedali e la Procura competente, che sta indagando anche su questi aspetti della vicenda.
Nella scienza non si presuppone nulla: contano i dati, e nient’altro. Dati che Stamina Foundation sostiene – qui, oggi, nella figura del suo Presidente – di possedere.
Confido che vorrà condividere quanto prima questi dati, così rivoluzionari per la medicina rigenerativa.
be certo se sono in grado di produrre ogni tipo di cellula staminale possibile, in pratica Stamina possono guarire ogni tipo di morbo o malattia esistente, azzerare l’invecchiamento facendo rigenerare i tessuti all’infinito, produrre organi da trapiantare senza rigetto, ecc… quindi Gesù Cristo che “solamente” ridava la vista ai cechi e faceva camminare gli storpi era un dilettante in confronto a Vannoni!
Veramente , Signor Vannoni , queste immagini non dimostrano quello che lei vorrebbe far credere esattamente come le immagini da lei utilizzate per la domanda di brevetto .
La sua prolusione contiene un errore: la sifilide non è una malattia causata da un agente patogeno virale, ma da un batterio di tipo spirochetoide.
Domande: che tipo di cellule usate per preparare le iniezioni ai pazienti: quelle della figura 2, quelle della figura 4 oppure dipende da paziente a paziente? Come controllate che le cellule siano diventate neuroni? Oppure sono neuroblasti? Oppure sono cellule staminali neurali? E quante cellule del midollo osseo si sono trasformate? Tutte o solo alcune? Nel secondo caso, come fate a separare le cellule transdifferenziate da quelle che sono rimaste mesenchimali? Non inietterete mica un miscuglio di cellule diverse, vero?
Può darsi, in realtà mi pare che da qui ad elencare le cose come stanno ce ne passi e la cosa non è auspicabile in scienza – basti pensare alla vaghezza delle domande di brevetto in USA, non garantiscono né accuratezza né sicurezza.
Per questo è IMPERATIVO rivelare una buona volta questi protocolli e la metodica Stamina, sottoponendola alle analisi approfondite della comunità scientifica.
Chi non ha niente da nascondere non avrebbe problema a mettere tutto alla luce del Sole, no?
Alessandro Mattedi
Il treponema non è un virus
Peccato che l’attività telomerasica in cellule staminali dovrebbe essere alta per definizione.
[…] See on Scoop.it – The Matteo Rossini PostSono un ricercatore, impegnato da più di dieci anni in progetti di immunologia dei tumori e terapia genica. Nel momento in cui credo di avere raggiunto un risultato di rilievo, il mio primo pensier…See on noidiminerva.wordpress.com […]
può sembrare poco ma siccome viene eseguito un prelievo di midollo osseo e un seguente impianto sulla stessa persona o su altri soggetti viene eseguita la ricerca di WNV?
Vannoni “siamo infatti convinti che non si tratti di un solo tipo di cellule staminali, ma di più tipo con funzioni rigenerative differenti”
Convinti? CONVINTI??
Dopo quattro anni di attività avete solo una convinzione? Prima di somministrare qualcosa a qualcuno quantomeno dovreste essere CERTI di che cosa state somministrando!
Cercando di evitare le polemiche, siamo piú che convinti ed abbiamo già parecchi dati al riguardo, ma la ricerca che viaggiava parallela alle cure compassionevoli è stata interrotta dal ministero e dall’aifa dopo la visita ispettiva, quando hanno ordinato all’ospedale quali erano i cd da considerare (già tutti presenti), limitando la quantità più ampia che stavamo usando noi (con non poche difficoltà perchè alcuni cd hanno gli stessi cromatismi e quindi non possono essere considerati contemporaneamente). Questa è la ragione per cui da Miami ci aspettiamo qualcosa di più che non rifare le caratterizzazioni già fatte a brescia. Appena avremo completato i dati procederemo con le pubblicazioni che fanno parte di un’area di ricerca di base. Il lavoro fatto da nostri biologi russi è stata solo l’apertura di una via (come spesso avviene nella ricerca). Per il resto le polemiche e le accuse non servono a nulla, soprattutto ad aprire una qualsiasi forma di dialogo.
Mi perdoni Dr Vannoni,
non mi è chiaro un passaggio.. Quindi state facendo ricerca di base quando è stata già avviata una terapia? Ci sono studi pregressi che diano informazioni riguardo cosa diventano queste cellule iniettate in un organismo, qualsiasi esso sia?
Perdoni l’ignoranza
Anche i farmaci antiepilettici non si sa esattamente come funzionino,però si somministrano ai pazienti.
Signor Vannoni, ma lei ha un’idea di cosa voglia dire eseguire un’analisi per individuare i diversi CD? Perché io sarò anche una studentessa con poca esperienza in laboratorio, ma so che individuare la presenza dei markers delle MSC non è così complicato come lei ci sta facendo credere, è questione di giorni. Per “cromatismi” non so quali di queste tre interpretazioni intendesse http://it.wikipedia.org/wiki/Cromatismo, forse la parola giusta era fluorocromo o fluoroforo? Se ha degli collaboratori che trovano difficoltose queste operazioni, le consiglio di affidarsi a qualcuno di più competente. E mi limito a contestare solo questo perché ho da studiare per curare davvero qualcuno, un giorno!
Per cromatismi si intedono i colori (più che wikipedia può usare un normale vocabolario). Se poi si fa spiegare, non da me, ma dai suoi colleghi studenti come funzioni un citofluorimetro, si accorgerà che la sovrapposizione CROMATICA è un problema per la lettura contemporanea di CD differenti. Quando i suoi amici studenti espertissimi avranno preso il PHD li farò discutere con i nostri biologi e magari potranno scambiarsi informazioni a pari livello.
sono d’accordo. La characterizzazione del CD profilo e una rutina che si fa in un giorno. E non c’e nessun problema nella sovrapposizone cromatica, i controlli lasciano risolvere questo problema in pochi minuti. pero qui i controlli non ci sono))
Come possiamo prendere sul serio una persona che scrive “brescia” ?
Mi piacerebbe sapere che tipo di Citofluorimetro utilizzate. Oggi in commercio ci sono dei citofluorimetri in grado di leggere fino a 18 colori ( cromatismi in citofluorimetria non si usa mai ) contemporaneamente…possibile che STAMINA ne sua sprovvisto?
Lettura interessante,che dire, il Sig. Vannoni è da lungo tempo al centro di questo caos mediatico legato alla faccenda Stamina, le risposte di questa persona sono da sempre evasive e meno che mai chiare. Tutte le persone allenate alle scienze mediche, sto parlando di Biologi,Medici, Biotecnologi e tutte le altre categorie che spero non me ne vogliano non cito, sanno che un affermazione nel nostro campo necessita di mille prove e controlli. Il Sig. Vannoni fino a questo momento, non hai mai divulgato dati che provano l’efficacia della sua terapia, vi prego non ditemi che i video delle Iene sono una prova, non sono neanche lontanamente un indizio. Spero che a sua volta non me ne voglia il Dott. Marangoni autore dell’articolo sopracitato, non credo sia corretto fare il referaggio a qualcosa che non è un articolo scientifico, cosi si fà il gioco della disinformazione poichè in questo modo si può dire tutto il contrario di tutto. Fino a questo momento, le pratiche adottate dallo Stato Italiano e dal Sig. Vannoni sembrano ai miei occhi insensata fantascienza, figlia di un credo populista instillato nelle persone attraverso media famelici e famiglie disperate. Potrei citare un infinità di articoli che mostrano come cellule staminali di qualsiasi genere embrionali, pluripotenti indotte, neurali o del midollo osseo hanno una potenzialità tumorigenica intrinseca, ma non è questo il punto (FONDAMENTALE) per cui il meotodo stamina mostra delle falle. Secondo quale modello le cellule staminali mesenchimali (gia a questo punto ci sono dei dubbia ma andiamo avanti) del Sig. Vannoni possono essere in grado di portare un migliormento a queste patologie: ”Malattie cardiache
Malattie autoimmuni
Malattia di Parkinson
Lesioni spinali
Lupus eritematoso sistemico
GvHD
Danni renali
Ictus cerebrale
Malattia di Alzheimer
Sclerosi multipla
Diabete Mellito di tipo I
Osteogenesi Imperfetta e diffetti osseo-cartilaginei
Degenerazione dei nuclei della base (MSA, PSP, Huntington, Tourette)
Transplantologia” http://www.staminafoundation.org Patologie cosi diverse con deficit a livelli di tessuti, organi, di tipo immunitario, cell autonomous e non cell autonomous?? Il Sig. Vannoni in passato ha mostrato la generazione di neuroni, mi chiedo, solo perche ha delle cellule con una protuberanza di tipo assonale, ciò non fa di quelle un neurone. Sarebbe come dire che far miagolare un ragazzino e fare di lui un gatto, non ha molto senso. Non voglio star qui a elencare centinai di marcatori che andrebbero indagati prima di poter affermare che quella cellula è possibilmente un neurone, perché anche a quel punto solo l’analisi dei marcatori non basterebbe, perché qualsiasi rivista scientifica per qualsiasi articolo chiederebbe l’analisi funzionale, quelle cellule sanno davvero fare quello che i neuroni fanno normalmente? Adesso arriva il bello, queste prove che vi ho elencato, che superano di molto quello che il Sig. Vannoni ha potuto mostrare fin ora non bastano, poichè, ciò che si vede in un modello ex-vivo non corrisponde necessariamente a ciò che accade in vivo, nel organismo. Queste sono solo alcune delle obiezioni che si potrebbero fare al metodo Stamina, probabilmente non sono neanche le peggiori. Per quel che un semplice Biologo come me può vedere, tutto ciò non basta per sottoporre questo protocollo a delle persone, lo trovo una scelleratezza che sfrutta la disperazione delle famiglie che si trovano in momenti difficili. Uno stato degno di questo nome non dovrebbe permetterlo. Riccardo De Santis
Si ci sono e ci sono centinaia di trial clinici sulle mesenchimali in giro per il mondo (una fatta dal dr. Uccelli), nonostante il fatto che, ancora oggi, il concetto di ‘mesenchimali’ non sia completamente svelato e vi siano posizioni contrastanti anche su alcuni CD che le dovrebbero caratterizzare con certezza (ad esempio il CD 105). La conoscenza perfetta di come agiscano e di come rigenerino i tessuti danneggiati è ancora una conoscenza imperfetta (come avviene in tutti i campi della scienza). La ricerca di base lavorerà ancora per i prossimi 100 anni prima di capire le varie sfumature in cui agiscono le cellule mesenchimali. Comunque questo è parte dell’imperfezione della conoscenza, non è cha abbiamo rinunciato a mandare gli uomini nello spazio solo perchè non abbiamo ancora chiaro il concetto di materia oscura…
Nel caso stamina ancora spesso si confonde il concetto di ricerca di base, di sperimentazione framaceutica e di cura compassionevole. Ripeto sono tre vie diverse con scopi, modalità e prerogative differenti (ed anche leggi a tutela specifiche). Adesso scusatemi, ma devo andare. Buon anno a tutti.
Dott. Vannoni, premesso che sono un profano in materia e che per quello visto in TV la stimo, perchè non pubblicare tutti i dati e mettere a tacere tutte le polemiche annesse? Le auguro un buon 2014 e spero che riesca a chiarire la vicenda nel minor tempo possibile.
P.S. : continui sempre con la stessa forza il suo lavoro
Esatto, continui a fare il suo lavoro: IMPRENDITORE E PROFESSORE DI PSICOLOGIA! La scienza lasciamola agli scienziati perfavore.
il concetto di “cellule mesenchimali staminali” e’ stato definito chiaramente e la definizione e’ stata pubblicata in Pubmed.
“nonostante il fatto che, ancora oggi, il concetto di ‘mesenchimali’ non sia completamente svelato e vi siano posizioni contrastanti anche su alcuni CD che le dovrebbero caratterizzare con certezza”
è per questo che fate sperimentazione direttamente sui pazienti?
Mah fare la ‘revisione’ di alcune pagine prese da FB come se fossero un paper neanche mi sembra che abbia molto senso ‘scientifico’… Cosa si voleva dimostrare?
Si potrebbe dire altrettanto che pubblicare delle immagini su fb non lo si possa ritenere una “prova sperimentale” della bontà del metodo Stamina. Detto questo, i grafici derivati dall’analisi tramite FACS possono essere commentati, da un punto di vista scientifico, anche se presenti in una slide.
Cito il l’esperto di comunicazione persuasiva Vannoni “La ricerca di base lavorerà ancora per i prossimi 100 anni prima di capire le varie sfumature in cui agiscono le cellule mesenchimali.” Così si sottovaluta, Professore! Tra 100 anni la sua metodica avrà debellato tutte le malattie genetiche ad oggi scoperte! Ma che dico, tra 10 anni al massimo, saremo tutti degli ex malati di parkinson che ballano il tip-tap! Mai più ictus e parkison, giusto? Deve solo sperare che i video e le brochures che propinava alle sue inermi cavie non finiscano in mano alla procura (se già non è così).
L’unico modo per aquisire credibilita’ nella comunita’ scientifica e’ di pubblicare i propri dati su riviste scientifiche dopo essere stati sottoposti ad un processo di peer-review, come giustamente Francesco spiega!
Se questo metodo e’ veramente in grado di aiutare malati incurabili fino ad oggi, giornali come Nature o Science sarebbero lietissimi di accogliere lo studio.
Perche’ questo non e’ stato fatto? Ora non sto parlando di capire tutti i complessimi meccanismi cellulari implicati (percui la ricerca di base avra’ ancora molto da fare) ma quantomeno dovrebbero essere disponibili dati che mostrano un significativo miglioramento su tot numero di pazienti seguendo un x protocollo, no? Finche’ gli studi non sono pubblicati (e non su facebook!) e’ normale che tutti sono contrari.
Noi ricercatori non siamo nessuno e non possiamo trovare nemmeno un lavoro senza pubblicazioni.
Ma forse il problema piu grande e’ che ora si concede ogni giorno sul telegiornale uno spazio per un argomento cosi delicato quando nemmeno si e’ sicuri che la tecnica funzioni! La gente non competente in materia va in confusione e visto che ci sono forti emozioni implicate (parlando di malati gravi) succede un casino!
Ma poi il bello e’ che anche se queste poche cellule fossero effettivamente staminali, anche se fossero prive di proprieta’ tumorali, anche fossero sterili e sicure, comunque non ci sono prove che si trasformino in neuroni. Ma anche se si trasformassero in neuroni, sarebbe come lanciare un mestolo e una ciotola in una cucina e sperare che ne esca una teglia di biscotti. Se i neuroni non arrivano in sede, sopravvivono e si integrano nella rete (o addirittura ripristinano collegamenti persi, come si desidererebbe per queste patologie) servono tanto quanto un due di picche quando briscola e’ fiori.
Vannoni, la scienza e’ certezza, non cazzate. E piantala con il “cure compassionevoli”, quelle secondo la legge italiana vanno somministrate GRATUITAMENTE, non a 40000 euro a botta.
Per non parlare della possibilità, per niente discussa fino ad oggi, di generare eventi autoimmunitari con effetti clinici quasi peggiori di alcune di queste patologie elencate.
In fin dei conti che cosa ci ha dimostrato questo lavoro fatto senza i controlli? Dove sono i metodi? Senza i metodi e i controlli il lavoro non e’ considerato scientifico.
L’unica cosa che possiamo supporre e’ che avete MSC nelle mani (con forzatura, perche’ per definire MSC prima di tutto deve essere dimostrato il potenziale delle cellule di differenziarsi nelle tre linee mesenchimale, che qui non e’ stato fatto, pero’ lasciamo perdere). Ma dopo di tutto che sorpresa e’ il fatto di avere le MSC? MSC si coltivano gia’ da 40 anni, e’ facilissimo ottenere e coltivare umane MSC. Basta solo fare prelievo dal illiac crest. Nel caso presente piu’ importante e’ dimostare il potenziale delle MSC differenziarsi in neuroni, perche’ questo tipo di differenziazione e’ una sfida per le cellule d’ origine mesenchimale. Neanche questo e’ stato fatto pero’ lasciamo perdere. Supponiamio che useremo queste cellule per infusione nell’ uomo. In questo caso e’ essenziale dimostrare che MSC non hanno il potenziale tumorogenico. Infatti, dai lavori pubblicati nel “Science” sappiamo che il cancro di stomacho e le sarcome possono essere originati dalle MSC. Poi ogni technico che lavora con le cellule staminali sa che dopo il coltivo in vitro le MSC cambiano il suo cariotipo e possono diventare pericolose. In teoria basta solo una tale cellula per originare il cancro. Cosi’, per studiare il potenziale tumorogenico non basta paragonare l’ attivita’ di telomerase nella popolazione totale di MSC e quella di una línea di cellule cancerose. Per la risposta definitiva tra gli altri devono essere fatti i test in vivo come gia’ e’ stato detto nel articolo. Aproposito, questo test (e anzi lo studio completo delle proprieta delle vostre cellule prima e dopo l’infusione) puo essere condotto nei diversi Lab scientifici validi d’ Italia, perche’ non chiederg li?
E poi, se rivolgiamo ai lavori originali di Vyacheslav Klimenko e Olena Shchegelska, vediamo che non hanno dimsotrato neppure loro che la sua popolazione di MSC si differenzia in neuroni. E’ interessante, come va adesso Klimenko, il suo Lab in Ukraina per caso non e’ stato chiuso?
ma che fa? copia e incolla dal web? tutti esperti qui…
Comunque ragazzi cerchiamo di mantenere la calma, evitiamo di degenerare nelle solite polemiche…
Io sono contrario al finanziamento del metodo Stamina per i punti oscuri e le incongruenze già mostrate più volte, ma se Davide Vannoni mi pubblicasse tutto liberamente dimostrando di poter ottenere in buona fede risultati, con tutto l’interesse a confrontarsi e a mettere a disposizione i dati sulla propria metodica, non avrei problemi a spezzargli una lancia a favore.
Perché risponde sempre Vannoni (letterato esperto di marketing online) e non uno dei suoi tanti biologi? Il merito di questa presunta scoperta come può essere di un uomo che l’ha fatta sua perché usata su se stesso (con pessimo risultato per una paralisi del VII nervo cranico)? E’ come se dicessi di aver scoperto il vaccino della polio perché sono stato vaccinato. Tutta questa storia non ha alcun senso.
Apprezzo molto l’approccio al problema ma il post perde efficacia se si considera che verrà letto da persone che non hano dimestichezza con il metodo scientifico, con la statistica e con il rigore in generale. Tra i molti esperimenti che non dubito siano stati fatti, la variabilità sarà pur esistita… la variabilità nei risultati è un dato essenziale, altrimenti chi può escludere che quell’esperimento sia l’unico su migliaia a mostrare ciò che si vuole vedere?
Questo lo scrivo giusto per far ragionare qualcuno che è portato a fidarsi di dati senza controlli o senza analisi statistica, però è anche vero che spesso il sig Vannoni si riferisce a “cure compassionevoli”… in esse la statistica è relativa… ed anche questo è un argomento trascurato.
Questa è probabilmente solo una “cura compassionevole”, o un rituale complesso che faccia sentire i malati accuditi e “curati” con le metodiche più avanzate. Un elaborato e costoso placebo.
Se così fosse avrebbe dell’ingegnoso… dell’ammirevole… potrebbe persino essere efficace in alcuni casi. Certo nella pratica attuale, pesantemente normata per la massima sicurezza dei pazienti, sarebbe una stranissima anomalia (di fatto le è). Sembrerebbe l’equivalente moderno di una danza sciamanica… Ammettiamo sia innocua, però si pone il problema dei costi costi sottratti a ricerca rigorosa ed a cure rigorose (forse in Italia troppo spesso carenti degli aspetti compassionevoli). Purtroppo ho letto che i pazienti trattati e le loro famiglie pagano profumatamente questi trattamenti… è così?
Le famiglie dei pazienti, prima di entrare in cura, sono obbligate a firmare un documento in cui si impegnano a non pagare nulla per le cure che verranno somministrate.
Gentile Prof. Vannoni,
la ringrazio per essere intervenuto nella discussione. Essa, pur essendo condotta tramite vie inidonee alla scienza come Facebook e giornali online, può diventare un’utile occasione per capirci vicendevolmente. Per il pubblico infatti, costituisce uno strumento per elaborare autonomamente un’opinione informata sulla solidità scientifica di Stamina. Ancor di più per lei, Prof. Vannoni, essa può costituire una via per superare almeno in parte lo scetticismo che circonda la sua metodica.
Ho apprezzato le sue risposte alle perplessità tecniche che ho espresso nella mia disamina, ma come si sarà già reso conto, gli scienziati credono solo ai dati presentati nero su bianco. Caldeggio quindi che lei possa ripubblicarli, completati almeno con gli opportuni controlli negativi e con le analisi statistiche della vitalità cellulare e dell’espressione dei marcatori mesenchimali.
Converrà però con me che tali dati, seppure importanti, siano corollari ai veri nodi cruciali della vicenda:
1) mostrare come le cellule trattate con metodo Stamina possano differenziare in neuroni e rimpiazzare quelli danneggiati dalle patologie neurodegenerative che si propone di curare;
2) che tali cellule non siano tumorigeniche in vivo, un’analisi che va ben oltre la misurazione dell’attività telomerasica in popolazioni di cellule in vitro.
L’ostilità che avvolge Stamina si incardina esattamente su questo: l’opinione pubblica a lei ostile crede che lei abbia fatto il passo più lungo della gamba, somministrando un trattamento prima di provarne adeguatamente le basi razionali, l’efficacia e la sicurezza, ai pazienti che più focalizzano la solidarietà della gente: i malati terminali pediatrici.
Faccio un parallelismo con la recente messa a punto di un’altra terapia avanzata: quella genica per la Sindrome di Wiskott-Aldrich. In quel caso, l’efficacia della terapia è stata dimostrata attraverso la riproduzione sia in vitro che in modelli animali della terapia che sarebbe stata somministrata al paziente (pubblicato nelle seguenti riviste: Molecular Therapy 2004 10:903; Human Gene Therapy 2006 17:303; Gene Therapy 2007 14:415; Molecular Therapy 2009 17:1073; Journal of Allergy and Clinical Immunology 2011 127:1376; Gene Therapy 2012 19:1150, elenco parziale). L’assenza di tumorigenicità è stata provata in diversi modelli animali di terapia, osservati per un lunghissimo periodo, escludendo in ogni caso che lo sviluppo di tumori fosse dovuto al trattamento sperimentale (Molecular Therapy 2009 17:1073; Molecular Therapy 2013 21:175). Tutto questo è stato fatto prima di passare all’uomo (Science 2013 341: 1233151).
Credo sia assolutamente necessario che lei convinca tutti della bontà della sua scienza. Se mostrasse i dati che qui le chiedo in modo convincente, porterebbe dalla sua parte gli scienziati –inclusi quelli che compongono i vari comitati scientifici-, con enorme beneficio per Stamina e per le persone che vi si affidano. Le chiedo di condividere tali dati con noi nella forma che riterrà più opportuna. Da parte mia assicuro che saranno rivisti e commentati nella più assoluta neutralità.
Francesco Marangoni
Egr dr Marangoni, come può immaginare condivido parzialmente le sue opinioni. Se da un lato è ovvio che solo la pubblicazione di dati può creare un riscontro critico nella comunità scientifica, dall’altro la vicenda Stamina ha avuto un decorso differente dal normale processo di validazione scientifica. A prescindere dal fatto che personalmente non condivido l’approccio farmacologico alle cellule staminali (anche se coltivate), trovo veramente difficile considerare il modello murino come affidabile soprattutto se viene utilizzato somministrando cellule staminali umane differenziate o meno. Le applicazioni sui 34 pazienti di Brescia rientrano in una legge italiana sulle cure compassionevoli ‘al di fuori della sperimentazione’ (cito il titolo della legge), e sono in linea con i principi generali previsti dalla legge europea (che a sua volta contiene un paragrafo relativo alle cure compassionevoli ed alla libertà di ogni stato di scegliere come applicarle). Il fatto che il prof. Ferrari chiamato a fare il presidente del nuovo comitato scientifico che dovrebbe presiedere alla sperimentazione del metodo Stamina, abbia deciso di partire dalla valutazione dei 34 pazienti in cura Brescia (alcuni, nonostante le interruzioni dell’Agenzia Italiana del Farmaco, ormai da quasi 3 anni) è un aspetto significativo che non ho sentito pronunciare da nessuno scienziato nostrano. Insomma se 34 persone affette da malattie rare sono state in trattamento per un periodo ampio di tempo, possibile che a nessun neurologo o esperto di malattie rare interessi sapere come stanno? Nessuno vuole vedere se hanno sviluppato tumori cerebrali? O se hanno avuto miglioramenti? O se si è modificato il decorso della malattia? Ipotizziamo che Stamina sia un soggetto passivo, che non ha mezzi neppure per fare valutazioni in proprio dei risultati ottenuti dai pazienti, perchè nessuno (compreso l’ospedale che somministra le cure, dopo aver ricevuto numerose indicazioni dagli enti nazionali preposti alla tutela della salute) ha valutato i pazienti se non per la sola assenza di effetti collaterali (che comunque è già qualcosa)? Vede nei numerosi anni in cui ho fatto il ricercatore e nel mio ruolo di docente universitario, seppur di altra estrazione e formazione, mi hanno insegnato che non è negando l’esistenza di un fenomeno che si ottengono delle risposte. Le cure compassionevoli (o per essere precisi non ripetitive) sono una realtà, nei prossimi mesi entreranno in cura altri 150 pazienti, perdere l’occasione di valutarli nel loro percorso terapeutico la trovo una bestialità immensa che rinnega lo scopo della scienza. Poi si può anche non essere d’accordo con la legge Turco/Fazio, si può anche dire che il comitato etico di Brescia che ha approvato le terapie è composto da una manica di lestofanti, ma non è con le preclusioni ed i pregiudizi che si ottengono risposte. I dati completi sulle cellule ottenuti a Brescia e le integrazioni che produrremo a Miami con il team di Camillo Ricordi saranno pubblicati integralmente e quindi visibili a tutti. A quel punto cercheremo i fondi per dei neurologi specilizzati nelle singole patologie che trattiamo per fare delle valutazioni serie e approfondite sui pazienti e che saranno oggetto anche queste di pubblicazioni di case report. Sinceramente riniziare dai topi, tenendo conto che non condividiamo tale approccio, lo troverei uno spreco di tempo rispetto a quella che è l’attività della mia fondazione (che non è nè un ente di ricerca, nè una azienda farmaceutica). Le dico peraltro che ciò è stato condiviso dal parlamento italiano che ha previsto una sperimentazione breve (18 mesi) del metodo Stamina partendo direttamente sull’uomo. La scienza è uno strumento per conoscere, è un metodo. La sperimentazione farmaceutica è un’altra cosa e se lei è intellettualmente onesto, come credo, questa distinzione la conosce benissimo. Se Stamina sopravviverà a tutto ciò non cambierà il metodo scientifico, ma forse riuscirà a modificare alcune delle regole della sperimentazione farmaceutica applicata al campo delle staminali che non è un problema sollevato solo da Stamina, ma da molti scienziati in tutto il mondo. Se poi condivide l’approccio di Carlo Croce dell’Università di Pittsburg che sta facendo ogni possibile pressione perchè Camillo Ricordi non faccia neppure la caraterizzazione delle cellule prodotte da Stamina, allora benvenuti nella nuova santa inquisizione. Ricordo però che la gente non è analfabeta, ma questa battaglia fondata sui pregiudizi di alcuni scienziati contro Stamina, che nascondono serissimi conflitti di interesse, sta minando la fiducia nelle istituzioni italiane e sta facendo percepire un abuso di potere a chi cerca una speranza secondo la legge italiana. L’approccio di Stamina lo si può condividere o meno, ma in questo caso non siamo più nel campo della scienza, ma in quello della politica, delle attività regolatorie e dei sistemi economici che le governano. Attenderò con interesse le sue valutazioni degli articoli che pubblicheremo.
Gentile Prof Vannoni. Sono molto stupita a leggere quanto scrive :”Insomma se 34 persone affette da malattie rare sono state in trattamento per un periodo ampio di tempo, possibile che a nessun neurologo o esperto di malattie rare interessi sapere come stanno? Nessuno vuole vedere se hanno sviluppato tumori cerebrali? O se hanno avuto miglioramenti? O se si è modificato il decorso della malattia?”.
Ma non dovrebbero esserci delle dettagliate cartelle cliniche su questi pazienti? Nessun neurologo ha visitato i pazienti durante il trattamento??
Purtroppo i dati raccolti sui pazienti (tuttora in cura) sono stati raccolti da due neurologi indipendenti le cui spese sono state sostenute da due associazioni di malati. L’ospedale dopo aver raccolto i dati dei primi pazienti, dopo il blocco dell’Aifa ha valutato la sola assenza di effetti collaterali. Il comitato scientifico dell’Associazione italiana Niemann Pick in cui era presente anche un membro del vecchio e bocciato comitato scientifico ministeriale, su richiesta degli iscritti (di cui ne abbiamo in cura quasi la metà) si è rifiutato di fornire un protocollo di valutazione della patologia. Direi che questo quadro ha poco a che vedere con la scienza.
La necessità di sperimentare le terapie a base di cellule staminali con regole analoghe a quelle dei farmaci, così come la necessità di sperimentare in vivo dette terapie, non è qualcosa che possa essere liquidata con semplicità, limitandosi a “non condividerla”.
Le cellule staminali, per loro natura, assomigliano infatti molto di più a farmaci che a organi da trapianto. Questo perché per le staminali valgono gli stessi dubbi e le stesse incognite che valgono per i farmaci: qual’è il dosaggio giusto? Qual’è il modo più adatto per somministrarle? Raggiungono il luogo in cui devono agire? In quantità adeguate? Agiscono nel modo corretto? Raggiungono luoghi che non dovrebbero raggiungere? Agiscono in modo potenzialmente dannoso? Eccetera eccetera.
Che piaccia o no, che faccia comodo oppure no, per rispondere a queste domande servono ricerche analoghe a quelle richieste per i farmaci, comprese le prove in vivo di efficacia e di tossicità.
Lei giustamente ricorda che la Scienza è una forma mentis, non un insieme di riti fini a loro stessi. Proprio per questa ragione non può limitarsi a “non condividere”: deve fornire delle risposte a quelle domande. Se non le vuole fornire attraverso le procedure già ampiamente collaudate, perché non le condivide, dovrà farlo in qualche altro modo. Ma deve farlo. “Non condividere” non è una scusa per non tentare neppure di verificare efficacia e pericolosità di una possibile terapia *prima* di proporla a persone malate.
E qui veniamo al secondo punto. In un post più sopra Lei invita giustamente a non fare confusione tra ricerca di base, sperimentazione clinica e cura compassionevole. Questa confusione, però, l’ha fatta proprio Stamina Foundation.
Che cosa ha offerto la vostra fondazione dal 2009 a oggi?
Ricerca di base? No, visto che fin da subito avete somministrato il trattamento ai vostri clienti.
Sperimentazione clinica? Neppure, visto che non vi siete mai preoccupati di raccogliere in modo sistematico le storie cliniche dei vostri clienti. Lei trova forse sorprendente «che a nessun neurologo o esperto di malattie rare interessi sapere come stanno» i pazienti. Perché dovrebbero? Siete voi a proporre la cura, non fantomatici neurologi “altri”. È invece a dir poco stupefacente che proprio a Stamina Foundation non si sia mai interessata saperlo come stavano i suoi clienti; che non si sia mai preoccupata di raccogliere dati in modo sistematico; che dal 2009 ad oggi non abbia mai fatto uno straccio di sperimentazione clinica, pur avendo trattato svariate decine di pazienti.
Cure compassionevoli, forse? E come è possibile ciò, se non esistono dati clinici sul rapporto rischio/beneficio del Metodo Stamina? Quali informazioni avete fornito agli Spedali Civili per ottenere l’autorizzazione a trattare i pazienti? Perché queste informazioni, a distanza di due anni, non sono mai state pubblicate? È demenziale dover aspettare la conclusione delle indagini della Procura per saperlo… (sì, ci sono indagini in corso anche a Brescia)
Perché se si vuole proporre il Metodo Stamina come cura (compassionevole o meno che sia), allora si devono avere dati specifici riguardanti il Metodo Stamina, magari parziali, ma devono esserci. Almeno sulla potenziale pericolosità. Non ci si può appoggiare a studi fatti da altri, su altri tipi di cellule staminali, ottenute con modalità diverse e usate in modi differenti.
Sarebbe come pretendere di somministrare il ketoprofene sulla base dei dati clinici di paracetamolo, ibuprofene e acido salicilico. Sempre FANS sono, ma l’efficacia di uno, nulla dice sull’efficacia degli altri. Per cui, non ha senso citare le «centinaia di trial clinici sulle mesenchimali in giro per il mondo», perché qui non è in discussione il potenziale medico delle staminali tout-court, ma i rischi e i benefici di quelle particolari staminali ottenute e somministrate secondo le modalità di Stamina Foundation. Sono questi i dati che continuano a mancare, pur avendo Stamina Foundation iniziato a somministrare il proprio metodo a persone malate fin dal 2009.
Sulla base di quali dati presentate il Vostro metodo ai malati, in qualità di cura? Quali evidenze di efficacia e sicurezza avete in mano? Su quali evidenze Stamina Foundation può affermare di aver informato i propri clienti in modo corretto e completo sui rischi e sulle potenzialità del trattamento offerto?
Dunque il punto chiave della questione e’ che nessuno da quanto mi sembra di capire si e’ preoccupato (come sottolinea l’utente “worldoutsidereality” ) di raccogliere in modo sistematico le storie cliniche dei pazienti in trattamento.
Le cartelle cliniche non sono state tenute ne dalla struttura ospedaliera dove il trattamento e’ stato eseguito ne da Stamina Fundation.
Se e’ cosi’, ora e’ dura dimostrare l’efficacia della terapia senza documenti e cartelle cliniche alla mano.
Pero’ basterebbe che le famiglie dei 34 bambini si recassero dai neurologi o esperti in malattie rare dove i figli sono gia’ stati visitati in precedenza (e dove quindi dovrebbero essere depositati i documenti con dettagliato quadro clinico prima del trattamento) e chiedere una visita ed una valutazione del miglioramento (sara’ pure a distanza di anni pero’ si puo’ valutare se il trattamento ha deviato in maniera significativa il decorso della malattia in mancanza di ogni terapia). Questi medici non possono negare una visita. Dati alla mano poi Stamina Fundation dovrebbe poi analizzarli e pubblicarli. Potrebbe essere fattibile?
Egregio Prof. Vannoni,
la ringrazio per la sua risposta. Comprendo che la priorità di Stamina Foundation è rendere disponibile il trattamento con cellule staminali mesenchimali agli ammalati di patologie neurodegenerative attraverso il canale delle terapie compassionevoli, sicuramente più veloce delle normali procedure di medicina traslazionale che richiedono una base scientifica imponente.
Voglio però portare la sua attenzione su un punto che considero fondamentale: anche le terapie compassionevoli necessitano di una base scientifica solida. Non lo sostengo solo io, ma anche il legislatore. Ad esempio, la legge Turco/Fazio art.1 comma 4 lettera a) rende disponibili tali terapie, in mancanza di alternative, *purché siano disponibili dati scientifici che ne giustifichino l’uso, pubblicati su accreditate riviste internazionali*. È proprio alla luce di questo principio che desidero riportare la discussione su un piano puramente scientifico, al fine di comprendere la base scientifica di Stamina. Le ripropongo quindi alcune domande che ad ora non hanno ricevuto una risposta esauriente.
1. La caratterizzazione immunofenotipica delle cellule non fornisce dati funzionali, che invece sono molto importanti. Le cellule trattate con metodo Stamina possono dare origine a osso, cartilagine e grasso? Se possono originare neuroni, con quale frequenza questo avviene?
2. Quali indicazioni *precliniche* avete sull’efficacia terapeutica delle cellule trattate con metodo Stamina?
3. Nodo sicurezza: prendo atto (senza condividere, me lo concederà) che considera gli esperimenti in vivo uno “spreco di tempo”. Ciò premesso, oltre all’attività telomerasica, quali altri test sono stati condotti per escludere la cancerogenicità delle cellule trattate con metodo Stamina?
4. Ovviamente sono molto interessato a dati clinici obiettivi sui pazienti, come indicato nella mia disamina originale, se me li potesse rendere disponibili.
La ringrazio sin d’ora per le sue risposte e per le informazioni scientifiche che vorrà condividere con noi. Ritengo davvero che questo dialogo costituisca un’occasione importante per capirci vicendevolmente.
Francesco Marangoni
in risposta a
Pierre Minesso
31 DICEMBRE 2013 ALLE 16:58
Anche i farmaci antiepilettici non si sa esattamente come funzionino,però si somministrano ai pazienti.
La invito a studiare:
http://www.ncbi.nlm.nih.gov/pubmed/8784210
Al contrario del metodo stamina, i farmaci antiepilettici sono stati estensivamente studiati in molti modelli sperimentali e la loro commercializzazione ha seguito lo svolgimento dei trials necessari prima di arrivare ad un paziente!!
[…] ricercatori hanno commentato i documenti pubblicati online sulle cellule degli spedali civili( http://noidiminerva.wordpress.com/20…li-su-stamina/ ) e hanno trovato inesattezze ma han pure detto che sarebbero mesenchimali, non altra roba. E poi […]
Il prof. Macchiarini, direttore dell’ Advanced Center of Regenerative Medicine al Karolinska Institutet di Stoccolma ha utilizzato (con successo) le cellule staminali mesenchimali per creare trachee bioingegnerizzate in cui si è rigenerata una mucosa con cilia mobili, e rigenerazione anche dei vasi. Anche lui -all’ inizio- ha subito critiche da parte di colleghi invidiosi, ma ha replicato con i dati obiettivi. E prima di intervenire sull’ uomo ha fatto ricerca per anni e anni sugli animali.
http://www.ncbi.nlm.nih.gov/pubmed/20730554
http://www.ncbi.nlm.nih.gov/pubmed/22405797
http://www.ncbi.nlm.nih.gov/pubmed/24161821
Adesso si sta dedicando alla rigenerazione del tessuto nervoso, ma sempre partendo dal lavoro in laboratorio e sugli animali, e pubblicando i risultati. Non su Facebook bensì su Biomaterials e su Lancet…
http://www.ncbi.nlm.nih.gov/pubmed/24215734
Io credo moltissimo nella terapia rigenerativa, ma fatta seriamente!
Ad oggi ho rintracciato due pubblicazioni riconducibili ad Andolina ed a Stamina Foundation, su una rivista Coreana:
http://pdf.medrang.co.kr/Ijsc/005/Ijsc005-01-10.pdf
http://pdf.medrang.co.kr/Ijsc/005/Ijsc005-01-11.pdf
Credo che una persona come te non ci metterà molto a notare il bassissimo valore dello studio..ma se puoi dacci un occhio.
La rivista OVVIAMENTE non ha impact factor, il che vuol dire che ha minore visibilità di altre..se Vannoni mi legge, mi può dire come mai in presenza di dati così apparentemente importanti non ha tentato di pubblicare su riviste più prestigiose?
Se legge il paragrafo cells supply si accorgerà che stamina non ha nulla a che fare con tale applicazione sia dal punto di vista clinico, sia per metodica di produzione cellulare
Gentile Dr. Vannoni, la ringraziamo per la battaglia di modernità e coraggio che sta portando avanti, siamo in tanti a sperare che lei non si arrenda mai. E’ assurdo vedere nei mass media “ricercatori” che pasticciano per anni su animali senza risultati (a parte i finanziamenti anche pubblici) che “si preoccupano” delle speranze dei malati e della loro sicurezza salvo poi utilizzarli (sia persone malate che sane)come cavie umane nel salto nel buio.. del salto di specie,che avviene durante i numerosi (e mai agli onori delle cronache) trial clinici,moltissimi dei quali fallimentari e dannosi quando non addirittura mortali, Molti malati e parenti di malati sono con lei.
Dott. Vannoni la ringrazio della risposta.
Vorrei farLe un’altra domanda.
Ascoltando l’intero intervento del Dott. Villanova alla conferenza delle famiglie dei pazienti mi è parso di capire che tra le ipotesi che quest’ultimo prende in considerazione appare più probabile un effetto di riabilitazione delle cellule esistenti piuttosto che la rigenerazione dei neuroni. Ho capito correttamente?
Non si tratta di una differenza ben sostanziale rispetto a quanto Stamina dovrebbe essere secondo i dati noti (es. la richiesta di brevetto)?
Grazie
Resta il fatto, comunque, che i metodi di divulgazione adottati da Stamina sono quantomeno curiosi. Se i dati ci sono e se sono coinvolti degli esperti, appare veramente inspiegabile la divulgazione “a spizzichi e bocconi” delegata di volta in volta alle Iene, alle conferenze dei pazienti, a Facebook, e mai alle dichiarazioni e ai testi dei biologi che Lei dice operanti nei laboratori per Stamina.
http://www.nature.com/news/stem-cell-fiasco-must-be-stopped-1.14375
a voi interessano parole,..magari anche sovvenzioni,brevetti, pubblicazioni su cui basare carriere,conferenze e cattedre.. a noi parenti di malati interessano i fatti ..i progressi fatti dai bambini sottoposti alla cura Staminal e che abbiamo visto in video sono FATTI.
A me -come medico- interessano i fatti documentati. Se delle centinaia di pazienti che sono stati trattati (in maggioranza adulti) non si sa niente, e vengono mostrati solo due bambini (sempre gli stessi) che sembra abbiano avuto dei miglioramenti (e se fosse stato un caso? Chi dice che non sarebbero migliorati lo stesso?) la cosa “puzza” un po’. A chiunque. E non si può rimproverare ai detrattori di non essere andati a controllare i risultati: se io propongo una terapia che ritengo efficace, sta a me dimostrare con i fatti che è vero. Non posso andare in giro a dire “Il 70% dei pazienti curati migliora sensibilmente” e mostrarne solo DUE.
Veramente ci sono anche i filmati del medico malato (adulto) mi pare del nord Italia che ha riaquistato la completa mobilità…se vuole le cerco il filmato e glielo mando..Cmq approfitto del suo intervento per farle alcune domande sugli attuali trial clinici che trovo ben più discutibili della questione Staminal(cura che peraltro si avvicina maggiormente al ramo trapianti che non alla prassi farmacologica..):
Per chi non lo sa La sperimentazione clinica di fase I comprende un insieme di studi sul VOLONTARIO (UMANO) SANO O AMMALATO,che riguarda la determinazione del profilo di tollerabilità e quello farmacocinetico‐metabolico di un farmaco..[…](regolamentato da DPR 439, 21 settembre 2001)
Art. 1. Ambito di applicazione:
Il presente regolamento disciplina le procedure per l’accertamento della composizione e dell’innocuità dei prodotti farmaceutici.
Articolo 3 Si definisce prodotto farmaceutico di nuova istituzione Un medicinale che:a)non sia MAI stato utilizzato nell’uomo[…]
Fasi della sperimentazione
• Fase I: consiste in un’accurata valutazione della
relazione dose-risposta in un piccolo numero di
VOLONTARI SANI (20-30)
• Fase II: comporta la valutazione del farmaco in un
piccolo numero di pazienti (100-200).Un placebo od
un farmaco di controllo già in uso vengono inclusi in
un protocollo a singolo o doppio cieco come termini
di paragone.
…………………………………………………………………………………
Fatta questa premessa che lei conosce bene, vorrei capire :1)quanto sia in linea con il giuramento di Ippocrate e con la sicurezza del paziente (di cui gli AntiStaminal sembrano preoccuparsi tanto) quando la PRASSI sia somministrare a volontari SANI molecole di cui non si sa nulla (nella specie umana) e che, cmq , essendo sani, hannno solo che da perderci a fare le cavie..qui sembra che la sicurezza del paziente SANO si possa sacrificare legalmente e senza levate di scudi per il bene della scienza, o no?
2) quanto sia etico, sicuro e giusto prevedere legalmente la sperimentazione umana in SINGOLO O DOPPIO CIECO..terra terra io, malato grave, firmo un consenso informato per provare su di me una nuova molecola e poi rischio che mi sia dia un placebo!!Meno male che vi preoccupate tanto per la vita dei singoli..almeno quando ci si deve scagliare contro Staminal…Sicuramente se qualsiasi paziente sapesse prima di firmare che, invece di provare una cura sperimentale al posto della cura attuale,per la sua malattia grave potrebbe prendere acqua e zucchero nessuno firmerebbe perchè si sentirebbe truffato!
Quindi ricapitoliamo: sperimentare novità su persone sane è legale e ben accetto , dare un placebo ad un malato che invece si aspetta delle cure (e firma per quelle, che siano nuove o vecchie) va bene,far firmare consensi informati adducendo dati animali che,in quanto tali, non ci dicono un gran che per l’uomo va bene, e invece sperimentare una nuova procedura su volontari malati che lo richiedono espressamente in piena coscienza ,forti del fatto che ci sono stati positivi riscontri su altri malati e che, sostanzialmente non ci sono danni peggiori a quelli che cmq incorrerebbero anche non prendendo nulla non va bene??????????????Se permette questo mi puzza da morire..se permette questa “sanità italiana” secondo me è da rivisitare un pò, se permette esprimo che odio che le mie tasse vadano in favore di questo assurdo sistema…(e , per questioni di spazio, non ho parlato dei conflitti di interesse tra finanziatori e finanziati, non ho parlato di chi compone i comitati etici,ecc, ecc)
@marmanu: Provo a rispondere ad alcuni suoi dubbi, più che legittimi.
«cura che peraltro si avvicina maggiormente al ramo trapianti che non alla prassi farmacologica..):»
Le incognite poste da un’infusione cellulare – come ho già spiegato in un mio intervento precedente – sono analoghe a quelle della somministrazione di un farmaco, non del trapianto di un organo. Quante cellule sono necessarie? (dosaggio) Quante raggiungono il luogo dove devono agire? Quante agiscono nel modo giusto? Quante nel modo sbagliato? Quante finiscono dove non dovrebbero? Fanno dei danni? (dinamica e cinetica). Certo, sarebbe meglio avere regole appositamente studiate per queste terapie molto particolari, con tutte le loro sfumature, ma in mancanza di esse, le norme farmacologiche sono di gran lunga le più appropriate.
Chiunque le abbia detto che la terapia con cellule staminali si avvicina al trapianto più che al farmaco, le ha detto il falso.
«1)quanto sia in linea con il giuramento di Ippocrate e con la sicurezza del paziente (di cui gli AntiStaminal sembrano preoccuparsi tanto) quando la PRASSI sia somministrare a volontari SANI molecole di cui non si sa nulla (nella specie umana)»
I test tossicologici pre-clinici su animali sono una delle pratiche di sperimentazione animale più collaudate ed efficienti. Allo stato attuale, la loro attendibilità sfiora il 100% (http://www.ncbi.nlm.nih.gov/pubmed/15906587). È quindi perfettamente compatibile con il giuramento di Ippocrate chiedere a dei volontari di sottoporsi a dei test con fattore di rischio bassissimo, ma che consentono di stabilire con la necessaria precisione il dosaggio del candidato farmaco che sarà possibile somministrare a persone malate, quindi più vulnerabili. Purtroppo troppo spesso questo “dosaggio massimo tollerabile” risulta troppo basso per aspettarsi un qualche effetto terapeutico, e il candidato farmaco verrà scartato già in questa fase. Altri verranno scartati più avanti, per ragioni analoghe. Questo è il motivo per cui pochissimi farmaci superano i trial clinici; la SA in tutto questo non c’entra più nulla perché ha esaurito le sue funzioni *prima* dei test clinici.
Ebbene sì, le pratiche di sperimentazione animale sono costantemente sottoposte a verifiche, la loro attendibilità è costantemente messa in discussione e, ogni volta che si rivelano inadeguate, vengono abbandonate.
Chiunque le abbia raccontato il contrario le ha mentito spudoratamente, e farebbe bene a riflettere profondamente sull’opportunità di continuare a fidarsi di chi si è permesso di mentirle in modo così becero e profondo su argomenti tanto delicati, magari con il solo fine di portare avanti un’agenda politica o economica (rigorosamente mascherata da no-profit).
«2) quanto sia etico, sicuro e giusto prevedere legalmente la sperimentazione umana in SINGOLO O DOPPIO CIECO»
Questo è un punto molto importante, sul quale ci si continua a interrogare. Non utilizzare il doppio cieco significa prendere cantonate colossali, come dimostra ad esempio il costante lavoro della Cochrane Collaboration, sempre attiva nello “stanare” pratiche mediche consolidate ma rivelatesi poi inutili (tra le più famose, ricordo qui l’episiotomia) . D’altra parte, il doppio cieco comporta il rischio di ritardare l’applicazione di una cura efficace in metà dei pazienti trattati. Conciliare queste due necessità non è banale, e non esiste una risposta univoca che vada bene in tutti i casi, dalla chirurgia ai vaccini. Attualmente le linee guida per l’allestimento di un trial prevedono, come regola generale, che a tutti i pazienti vengano comunque somministrate eventuali terapie efficaci già note. Inoltre, I dati raccolti vengono valutati *in tempo reale* da una commissione di valutazione apposita che, nel caso rilevi indicazioni di una efficacia della possibile terapia, può sospendere il doppio cieco e far sì che la terapia venga somministrata a tutti. Può inoltre sospendere la sperimentazione se si presentassero segnali di pericolo per i pazienti (come avvenuto di recente per un vaccino anti-HIV). Ogni protocollo però fa storia a sé, e deve essere costruito in base alla situazione contingente al fine di massimizzare i benefici per i pazienti; deve inoltre essere approvato da apposite commissioni etiche.
Di nuovo, la invito a riflettere profondamente sull’opportunità di continuare a fidarsi di chi si è permesso di descriverle il mondo della ricerca in modo così platealmente superficiale e fazioso.
«Sicuramente se qualsiasi paziente sapesse prima di firmare che, invece di provare una cura sperimentale al posto della cura attuale,per la sua malattia grave potrebbe prendere acqua e zucchero nessuno firmerebbe perchè si sentirebbe truffato!»
Tutti i pazienti reclutati per un clinical trial sono perfettamente al corrente di poter essere inclusi nel gruppo placebo, e che né loro né i medici che li seguono sono al corrente del gruppo di cui fanno parte, così come sono informati riguardo a tutte le evidenze già note di efficacia e potenziale pericolosità della cura (sottolineo *tutte* e *pericolosità*). Si chiama consenso informato. Quello che ci chiediamo qui – tra le altre cose – è se Stamina Foundation sia stata altrettanto scrupolosa nell’informare i suoi clienti circa le evidenze di efficacia e pericolosità del Metodo Stamina, e soprattutto sulla eventuale *mancanza* di evidenze e di sperimentazione.
Non so a quali fonti si sia affidato per comprendere il complesso mondo della ricerca biomedica, ma le rinnovo il mio invito a riflettere profondamente sull’opportunità di continuare a fidarsi di chi, fino ad ora, le ha palesemente raccontato un gigantesco, catastrofico fiume di balle.
Indipendentemente dalla buona fede o no di Stamina Foundation non ci si puo’ basare su 2 (o 3) video!
Ribadisco un concetto: se sono stati curati 34 pazienti perche’ non si valutano e pubblicano i loro quadri clinici con i significativi miglioramenti che i video mostrano?!?! (per tutti e 34 i pazienti pero’!!!)
Se Stamina Foundation non lo fa ci sono 3 spiegazioni:
1) sono masochisti,
2) la terapia non funziona,
3) sono poco seri e non si sono preoccupati di raccogliere in modo sistematico i dati sui pazienti. In quest ultimo caso ci sono comunque alternative per raccogliere i dati a posteriori (nel mio commento dei primi di gennaio ne ho proposto ona).
A noi interessa che i risultati vengano descritti in base a rigorosi e validati metodi di misurazione e statistici. Dispiace dirlo, ma un filmato non prova niente.
Federico,con tutto il rispetto..sai dove li metterebbero i kg di carteggi di misurazione statistica i genitori dei bimbi che ora, grazie a Staminal, muovono di nuovo braccine e gambine?
Se io sono malato terminale HO IL DIRITTO COSTITUZIONALE DI SCEGLIERE COSA FARE!Tanto le vostre tabellette per pubblicazioni, conferenze, cattedre e titoli le fate lo stesso, ma almeno lasciateci scegliere cosa fare della nostra vita!
Non per offenderla ma aspetterei le risposte dalla Dottoressa Lestuzzi…Intanto la rincuoro del fatto che, dalla mia formazione scientifica e,successivamente,in ambito legale, mi viene naturale destreggiarmi tra le onde dei “fiumi di balle” valutando in base a dati oggettivi, senza farmi fuorviare nè da “tifoserie” nè da altro che non lo stretto rigore logico.. Non a caso ho citato in premessa precisi regolamenti attualmente in vigore in Italia.(credo che lei non li abbia letti o non li abbia capiti visto che prima dice che i doppi ciechi servono, e poi dice che non vengono fatti perchè ai malati gli si assicurano le cure..delle due l’una..faccia chiarezza dentro di se).Oltre a ciò, (alle fonti lette e accumulate) purtroppo sono stata spettatrice impotente di un mio parente prossimo, affetto da cancro allo stomaco, che è stato incoraggiato a firmare un consenso (dis)informato per un trial x una nuova molecola (spacciando speranza attraverso miracolosi risultati raggiunti nei topi),morendo poco dopo (cioè in pochi giorni anzichè un anno..in punto di morte parlare di giorni o di anni conta sia per il paziente sia per i parenti)Sua moglie, al fievole tentativo di chiedere spiegazioni al personale medico che aveva seguito il marito si è sentita dire che si sapeva bene che i trial clinici sono rischiosi perchè uomini e animali sono diversi ma almeno il paziente aveva goduto di una speranza..(quindi nei trial clinici in nome della scienza mio zio è morto, e tanti come lui muoiono o non hanno effetti o hanno gravi controindicazioni e pazienza, perchè tanto morirebbero comunque..per la ricerca di Vannoni però questo discorso non vale?Perchè due pesi due misure? )
Tornando a mio zio,e alla risposta del ricercatore, era inevitabile inferocirsi sul fatto del perchè non si sia parlato nè di doppi ciechi, nè dell’enorme discordanza di dati in specie differenti..usate però per arrivare alla famosa firma….
Almeno Vannoni ed il suo staff hanno il merito di non “fuffare” le persone attraverso dati di altre specie..sà com’è..se sto morendo non è che mi interessi molto che nella capra tibetana ci sono stati riscontri incoraggianti..detto questo le consiglio di non giocare con le percentuali..o giocarci in maniera più credibile poichè la predittività dell 100% non la darei io (homo sapiens) ad un mio cospecifico malato di epilessia o di autismo, figuriamoci un topo o un ratto..
Aspettando fiduciosa le risposte della dottoressa le allego queste dichiarazioni( se vuole al prossimo commento le metto anche un pò di altre percentuali..):
Alan Oliff, ex direttore esecutivo per la ricerca sul cancro a Merck Research Laboratories nel West Point, Pennsylvania, USA, nel 1997 ha dichiarato: “Il problema fondamentale nella scoperta del farmaco per il cancro è che le i modelli [animali] non sono assolutamente predittivi” .
• nel 2006, l’allora Segretario della Sanità e Servizi Umani Mike Leavitt ha dichiarato: “Attualmente, nove farmaci sperimentali su dieci falliscono perché non possiamo prevedere come si comporteranno nelle persone sulla base degli studi di laboratorio su animali” .
• L’NCI ha dichiarato che la società potrebbe aver perso cure per il cancro a causa del modello animale .
• FDA statunitense sulla tossicologia ha affermato nel 1998 che “La maggior parte dei test sugli animali che accettiamo non sono mai stati validati.
• Salsburg ha commentato: “Così il tempo impiegato a condurre uno studio in topi e ratti sembra avere meno di un 50% di probabilità di trovare sull’uomo sostanze cancerogene note. Sulla base della teoria della probabilità, avremmo fatto meglio a lanciare una moneta .
• ”COME FAR CARRIERA SCEGLIENDO IL TOPO GIUSTO”, INTERVISTA AL PROF. CLAUDE REISS, biologo molecolare direttore per 35 anni del CNRS di Parigi ed attuale direttore emerito dello stesso, l’istituto di ricerca francese più importante , autore di centinaia di papers scientifici pubblicati sulle maggiori riviste di settore, consulente scientifico della commissione U.E D Prof. Reiss, sta dicendo che grazie ai test sugli animali si può provare una cosa ed anche il suo contrario?R Esattamente.
• Sausville, allora direttore associato della divisione del trattamento del cancro e la diagnosi per il programma di sviluppo terapeutica presso l’NCI ha dichiarato: “Avevamo praticamente scoperto composti che erano buoni farmaci per topi piuttosto che buoni farmaci per l’uomo”.
• In un articolo pubblicato su Fortune nel 2004, il Prof. Robert Weinberg, Professore di biologia al ”MIT” – Massachusetts Institute of Technology – una delle più importanti università di ricerca del mondo, con sede a Cambridge, nel Massachusetts, U.S.A. , vincitore della Medaglia Nazionale per la Scienza grazie alla sua scoperta del primo oncogene umano e del primo gene soppressore del tumore, dichiarò ufficialmente :”Uno dei modelli sperimentali del cancro umano più frequentemente usato è prendere cellule tumorali umane che vengono messe in coltura ,metterle in un topo immunocompromesso, x formare un tumore, e quindi esporre lo xenotrapianto che ne risulta a vari tipi di medicinali che potrebbero essere utili nella cura delle persone. Ed è ben noto forse da vent’anni, che molti di questi modelli preclinici del cancro umano hanno pochissimo potere predittivo in termini della risposta degli esseri umani, cioè dei veri tumori umani nei pazienti. Malgrado le somiglianze genetiche e del sistema degli organi tra un topo e un uomo, le due specie hanno differenze chiave in fisiologia, architettura dei tessuti, tempi del metabolismo, funzione del sistema immunitario, sistema di segnalazione molecolare ecc. Quindi i tumori che sorgono in ognuno, sono vastamente diversi. Un problema fondamentale che dev’essere risolto nell’intero sforzo della ricerca sul cancro, in termini di terapie, è che i modelli preclinici del cancro umano, in gran parte, sono del tutto inadeguati. Sebbene le industrie farmaceutiche riconoscano con chiarezza il problema, non vi hanno però rimediato. E sarebbe meglio che lo facessero, se non altro perché ogni anno le industrie farmaceutiche sprecano centinaia di milioni di dollari usando questi modelli ”.
• Dr. Homer Pearce, ex direttore di ricerca e di indagine clinica presso il noto colosso farmaceutico ”Eli Lilly” ed attuale consulente di ricerca della stessa azienda:”I modelli murini sono dolorosamente inadeguati. Se considerate i milioni e milioni e milioni di topi che siamo riusciti a curare, e li confrontate con il successo relativo, o meglio l’insuccesso, che abbiamo ottenuto a livello clinico nel trattamento del cancro metastatico…capirete che per forza ci dev’essere qualcosa di sbagliato con quei modelli ”,
• Dr. Richard Klausner, ex direttore dell’US National Cancer Institute:” Abbiamo curato topi malati di cancro per decenni e semplicemente non ha funzionato negli esseri umani ”.
• articolo pubblicato su Plos Medicine dal Dr. JJ Pippin, fondatore e direttore della medicina cardiovascolare e ”medical imaging” presso la ”Cooper Clinic”, autore e co-autore di oltre 60 articoli e abstract che sono stati pubblicati sulle principali riviste mediche, è stato anche portavoce e relatore presso la ”American College of Cardiology” e la ”Society of Nuclear Medicine, U.S.A.”, attuale consulente scientifico presso il Physicians Committee for Responsible Medicine (PCRM) degli U.S.A,:”Le uniche persone che non sanno, nel 2005, che la ricerca sugli animali è irrilevante per le malattie umane sono quelli che non lo capiscono o coloro che ne beneficiano. Come medico, ricercatore clinico, ed ex ricercatore animale, so che benchè siano i nostri parenti genetici più stretti, i primati hanno fallito come modelli di ricerca praticamente ogni volta che sono stati utilizzati a tale scopo. Si lamentava: “Abbiamo curato topi malati di cancro per decenni, e semplicemente non ha funzionato negli esseri umani”,l’Aids è un altro: mentre almeno 80 vaccini sono stati testati sugli animali, tutte e 80 hanno fallito il trial in pazienti umani. Allo stesso modo, ognuno degli oltre 150 trattamenti di ictus trattati con successo negli animali non hanno avuto i medesimi risultati nei test umani.
• «abbiamo avuto un sacco di modelli che non erano predittivi, che erano [infatti] gravemente fuorvianti”, dice Marks del NCI, consorzio di tumori Umani .
• Neancy Andreasen, psichiatra americana tra i massimi esperti mondiali sulla schizofrenia, dice “Non è possibile avere modelli animali per i disturbi del pensiero formale..Anche i modelli animali utilizzati dalle case farmaceutiche per testare l’efficacia terapeutica degli antipsicotici non sono validi.
• Kathy Archibald, scienziata genetista britannica già ricercatrice farmacologica, autrice di numerosi articoli scientifici e direttrice di Safer Medicines, concorda nel ricondurre ai modelli animali gli attuali problemi legati allo sviluppo di farmaci sicuri ed efficaci per il consumo umano:”La mia risposta alla domanda ‘se un trattamento funziona su roditori,ci curerà?’ è ‘probabilmente no, basata sul peso delle prove raccolte finora’.
• Khanna e Scott (2011) a proposito di sistema immunitario e ricerca sui modelli murini: “per quanto tempo possiamo andare avanti ad investire denaro pubblico per effettuare studi che non porteranno mai a risultati concreti in termini di applicazioni cliniche? “
• Hartung (2009) nel suo articolo pubblicato sulla rivista Nature “Tossicologia per il XXI secolo” che il modello animale è del tutto inadeguato per la valutazione del rischio tossicologico e che urge un cambio di direzione verso l’impiego di metodologie avanzate in vitro ed in silico, che potrebbero attualmente fornire risultati più sicuri ed affidabili.
• A seguito di 20 anni di ricerca sull’ipertensione usando animali geneticamente modificati che non hanno portato a nulla, Stingl, Völkel e Lindl hanno affermato:“Perciò, anche se questi approcci sono ritenuti senza eccezione “molto promettenti” in letteratura, non ci si può aspettare che la ricerca sugli Organismi Geneticamente Modificati rechi alcun contributo ad una nuova strategia terapeutica.
«prima dice che i doppi ciechi servono, e poi dice che non vengono fatti perchè ai malati gli si assicurano le cure..delle due l’una..faccia chiarezza dentro di se»
No, non ha capito. Il doppio cieco si fa eccome. Terapia normale+placebo vs. terapia normale+candidato, come regola generale. Poi bisogna valutare la situazione caso per caso. Il doppio cieco viene sospeso solo nel caso in cui emerga evidenza di efficacia prima della fine della sperimentazione.
Mi spiace che un suo parente sia rimasto coinvolto in un caso di palese misconduct (e forse anche qualcosa di peggio). Sono fatti gravi che andrebbero sempre denunciati. Tuttavia il fatto che ci sia chi non rispetta le regole, non dice gran che sull’efficacia delle regole stesse, quando vengono rispettate.
Inoltre le frasi che ha copincollato – al netto della propaganda ideologica – in realtà, se viste all’interno del loro contesto, dimostrano proprio quello che sto sostenendo io: la comunità scientifica si interroga costantemente sull’efficacia e sull’attendibilità delle pratiche di SA, e scarta quelle che dimostrano di non funzionare.
Per quanto riguarda le statistiche, sono lì da vedere.
Su 1559 soggetti trattati «The overall incidence of AEs was 8.8% with no significant difference between those occurring with active drug and those on placebo». Nessuna differenza significativa. I test tossicologici pre-clinici hanno consentito di stimare un dosaggio di sicurezza per le nuove molecole studiate, attendibile nel 100% dei casi.
I dati oggettivi sono questi, non c’è proprio nulla con cui giocare. Se lei non vuole accettarli, è un problema suo.
“The good thing about science is that is true, whether or not you believe in it” (Neil DeGrasse Tyson)
Confermo: le hanno raccontato un fiume di balle. Io più che presentarle un po’ fatti non posso fare: lo sforzo per scrollarsele di dosso, queste balle, lo deve fare lei. Nessuno la può aiutare.
ecco il vostro “cientopeciento”:
FORANE(anestetico) …Gravidanza: studi fatti sul ratto non hanno mostrato alcun effetto nocivo sulla fertilità, la gestazione, il parto e sulla vitalità dei nati. Medesimamente, esperimenti fatti sui conigli hanno prodotto coniglietti vitali, nonchè uno sviluppo fetale normale. Si ignora se il risultato di questi studi sia applicabile all’uomo. Poichè non esiste esperienza valida sulla donna incinta che abbia ricevuto questo farmaco non è stato possibile stabilire la sua sicurezza nella gravidanza”.
RETROVIR:
…Non si conosce quanto i risultati di carcinogenesi nei roditori siano predittivi per l’uomo.
CYTOTEC:
…Un aumento reversibile nel numero di cellule epiteliali gastriche di superficie normale si è verificato in cani, ratti e topi. Nessun aumento si è osservato in uomini a cui era stato somministrato Cytotec per un anno.
CEFOBID :
…Gravidanza: Studi sulla riproduzione sono stati condotti su topi, ratti e scimmie in dosi anche 10 volte maggiori rispetto alla dose per l’uomo e non hanno rivelato evidenza di infertilità o danno ai feti . Non ci sono tuttavia studi adeguati e ben controllati su donne incinta. Dato che gli studi sulla riproduzione negli animali non sono predittivi della risposta umana, questo farmaco deve essere usato in gravidanza solo se strettamente necessario.
AIRCORT spray nasale (budesonide) (contro le riniti allergiche)
..Gravidanza:la somministrazione del budesonide durante la gravidanza dovrebbe essere evitata a meno che non sussistano particolari motivazioni. Gli studi condotti negli animali hanno evidenziato effetti teratogeni variabili in funzione della specie animale. Poiché l’attinenza all’uomo di quanto osservato nell’animale non è stata ancora stabilita, nelle donne in gravidanza si sconsiglia l’uso di AIRCORT spray nasale soprattutto nei primi tre mesi di gestazione.
ZANTIPRES 7.5 mg compresse (trattamento dell’ipertensione arteriosa) luglio 2003
Dati preclinici di sicurezza: […] Nello studio di carcinogenesi condotto nel topo si è verificato un aumento dell’incidenza dell’atrofia testicolare; la rilevanza clinica di questo fenomeno non è conosciuta.
PRITOR 80 mg compresse (trattamento dell’ipertensione essenziale) maggio 2002
Dati preclinici di sicurezza: […] Nel cane sono state osservate dilatazione ed atrofia dei tubuli renali. Nel ratto e nel cane sono state osservate inoltre lesioni della mucosa gastrica (erosioni, ulcere o infiammazioni). […] In entrambe le specie sono stati osservati aumento dell’attività della renina plasmatica e ipertrofia/iperplasia delle cellule iuxtraglomerulari renali. Tali alterazioni anch’esse un effetto di tutta la classe degli ACE inibitori e di altri antagonisti dell’angiotensina II, non sembrano avere significato clinico.
ONCO-carbide (leucemia mieloide cronica) giugno 2000
Avvertenze speciali – Il prodotto, come la maggior parte dei farmaci antitumorali, ha dimostrato proprietà cancerogena negli animali, in particolari condizioni sperimentali.
OPTRUMA Raloxifene cloridato (prevenzione dell’osteoporosi nelle donne dopo la menopausa) ottobre 2001
Dati preclinici di sicurezza: […] Studi su ratti e topi hanno mostrato un aumento dei tumori ovarici trattati con alte dosi di farmaco. In questi studi, i roditori di sesso femminile, furono trattati durante tutta la loro vita riproduttiva, quando le loro ovaie erano funzionali ed altamente sensibili alla stimolazione con ormoni sessuali. In contrasto all’elevata sensibilità delle ovaie in questo modello di roditore, l’ovaio umano dopo la menopausa risulta relativamente insensibile alla stimolazione con ormoni sessuali.
Cardirene (prevenzione della trombosi coronarica) Gravidanza:
– nell’animale: è stato osservato un effetto teratogeno.
– nell’uomo: in base a molteplici studi epidemiologici (in particolare uno studio prospettico in un alto numero di donne) non è stato riscontrato alcun effetto teratogeno a seguito di somministrazioni saltuarie durante il primo trimestre di gravidanza.
Entocir
(trattamento del Morbo di Crohn) […] In un ulteriore studio non è stato confermato l’aumento dell’incidenza di gliomi nel cervello di ratti di sesso maschile che si era verificato in uno studio di carcinogenesi, in quanto l’incidenza di gliomi non è risultata diversa nei vari gruppi trattati con diversi principi attivi (budesonide, prednisolone, triamcinolone acetonide) e nei gruppi di controllo.
Le alterazioni epatiche (neoplasie epatocellulari primarie) rilevate nei ratti di sesso maschile in un primo studio di cancerogenesi sono state confermate in un ulteriore studio sia con budesonide, sia con altri glucocorticosteroidi di confronto. Tali effetti sono probabilmente dovuti ad un effetto recettoriale ed è quindi tipico della classe terapeutica.
L’esperienza clinica fino ad oggi acquisita non indica che budesonide o altri glucocorticosteroidi inducano gliomi cerebrali o neoplasie epatocellulari primarie nell’uomo.
La tossicità di ENTOCIR capsule sul tratto gastrointestinale è stata studiata nella scimmia cynomolgus dopo somministrazione per via orale di dosi ripetute fino a 5 mg/kg (circa 25 volte la dose giornaliera consigliata nell’uomo) per un periodo fino a 6 mesi. Non è stato osservato alcun effetto sul tratto gastrointestinale, né all’analisi macroscopica né a quella istopatologica.
Gravidanza: La somministrazione di budesonide come di altri glucocorticosteroidi nell’animale gravido causa anomalie dello sviluppo fetale. La rilevanza di tali osservazioni per l’impiego nell’uomo non è ancora stata stabilita.
ECOVAL Scal Fluid (Betametasone valerato) Gennaio 2004
Categoria farmacoterapeutica: CORTISTEROIDI ATTIVI (III GRUPPO). Indicazioni terapeutiche: dermatosi delle parti pilifere quali: dermatite eczematosa, eczema seborroico, psoriasi, alopecia areata, pitiriasi secca.
Gravidanza :La somministrazione topica dei cortisteroidi ad animali gravidi può causare anormalità nello sviluppo fetale. La rilevanza di questo dato sperimentale non è stata constatata nell’uomo
CLOBESOL 0,5 mg/g crema – 0,5 mg/g unguento (Clobetasolo propionato) Febbraio 2003
Categoria farmacoterapeutica: CORTISTEROIDI MOLTO ATTIVI (IV GRUPPO). Indicazioni terapeutiche: Dermatopatie quali psoriasi (esclusa la psoriasi a placche diffusa), gli eczemi recidivanti, il lichen planus, il lupus eritematoso discoide.
Gravidanza :La somministrazione topica di cortisteoridi durante la gravidanza negli animali da laboratorio può provocare anomalie nello sviluppo fetale. La rilevanza di questo dato sperimentale non è stata constatata nell’uomo.
ANTACAL :( amplodipina, trattamento ipertensione)
Uso in gravidanza ed allattamento
Studi sulla riproduzione animale hanno dimostrato che l’amlodipina non ha effetti tossici, ad eccezione di parti ritardati e prolungati nei ratti a dosi 50 volte maggiori della dose massima raccomandta nell’uomo.
Non essendo però stata ancora accerta la tollerabilità dell’amlodipina nelle donne in gravidanza o durante l’allattamento, l’uso del prodotto, in tali circostanze, è controindicato.
Megestil 160mg
(trattamento palliativo del carcinoma della mammella o dell’endometrio in fase avanzata, della sindrome anoressia-cachessia da neoplasia maligna in fase avanzata e da AIDS)
La somministrazione di megestrolo acetato a cani femmina per un periodo fino a 7 anni ha evidenziato un aumento di tumori mammari sia benigni che maligni. Al contrario, in studi comparativi nei ratti e in studi nelle scimmie, l’incidenza tumorale non e’ aumentata.
Benche’ la correlazione tra tumori canini e umani non sia ben nota, essa dovra’ essere tenuta in considerazione sia per la valutazione del rapporto rischio/beneficio nella prescrizione di Megestil che per il monitoraggio della paziente.
Isoptin
(insufficienza coronarica acuta e cronica, tachicardia parossistica, tachiaritmia, extrasistolia)
Novembre 2004
AVVERTENZE SPECIALI
Poiche’ gli studi sulla riproduzione nell’animale non sono sempr e in grado di fare prevedere la risposta nell’uomo, il farmaco deve essere usato durante la gravidanza solo se e’ strettamente necessario.
Krinuven senza elettroliti
(nutrizione per via parenterale in pazienti adulti quando la somministrazione orale o enterale non e’ possibile) Febbraio 2004
Gravidanza e allattamento:
La valutazione dei dati ricavati dagli animali ha mostrato tossicita’ riproduttiva dopo la somminisrtrazione di Structolipid. Le rilevanze cliniche di questi dati sono sconosciute.
Zyloric
(manifestazioni cliniche di deposito di acido urico/urato) Luglio 2005
Interazioni – Tolbutamide:
E’ stato dimostrato che la conversione della tolbutamide a metaboliti inattivi e’ catalizzata dalla xantino-ossidasi del fegato di ratto. L’eventuale rilievo sul piano clinico di queste osservazioni non e’ noto.
Miflonide 200 e 400
(asma bronchiale) Febbraio 2000
Gravidanza ed allattamento: Negli animali gravidi la somministrazione di corticosteroidi ha dimostrato causare anormalita’ nello sviluppo fetale. Non e’ ancora stata stabilita l’importanza di questo dato per l’uomo.
Zofran
(controllo della nausea e del vomito indotti da chemioterapia)
Luglio 2003
AVVERTENZE SPECIALI:
La sicurezza dell’Ondansetron in gravidanza nella specie umana non e’ stata stabilita. La valutazione degli studi sperimentali nell’animale non indica effetti dannosi diretti o indiretti sullo sviluppo ambrio-fetale, sulla gestazione e sullo sviluppo peri e post-natale. Tuttavia, poiche’ gli studi nell’animale non sono sempre predittivi delle risposte nell’uomo, ZOFRAN non deve essere somministrato in gravidanza.
Aldactazide 25 mg
(stati edematosi da iperaldosteronismo secondario) Luglio 2004
Avvertenze: Come altre sostanze che interferiscono con attivita’ ormonali, lo spironolattone somministrato a dosi molto piu’ elevate di quelle terapeutiche e per tempi molto prolungati, puo’ talora determinare nel ratto un aumento dell’incidenza di alcuni tipi di processi eteroplastici. Allo stato attuale delle conoscenze scientifiche non e’ possibile attribuire a queste osservazioni alcun sicuro significato per l’uomo.
Eutimil
(depressione, attacchi di panico, ansia) Luglio 2003
Gravidanza e allattamento:
Sebbene gli studi sugli animali non abbiano dimostrato alcun effetto teratogeno o embriotossico selettivo, la sicurezza della paroxetina nella donna in gravidanza non e’ stata stabilita.
Topmax
(epilessia) Febbraio 2004
Gravidanza e allattamento:
Il topiramato, al pari di altri farmaci antiepilettici, si e’ dimostrato teratogeno negli animali. Non vi sono studi sull’uso del topiramato in gravidanza. Dall’esperienza post-marketing, sono stati riportati alcuni casi di ipospadia nei bambini maschi esposti al trattamento con topiramato durante la gravidanza, anche in associazione con altri antiepilettici. Non e’ stata riconosciuta una correlazione causale diretta con topiramato.
Ecoval
(dermatiti) Febbraio 2006
Gravidanza e allattamento:
La somministrazione topica di corticosteroidi durante la gravidanza negli animali di laboratorio può provocare animalie nello sviluppo fetale. La rilevanza di questo dato sperimentale non è stata constatata nell’uomo.
Il ruolo della SA nella ricerca biomedica non è quello di rappresentare l’essere umano a 360º. Questa è una falsa idea (un vero e proprio straw man argument) propagandato implicitamente dagli anti-SA.
Ogni esperimento su animali ha lo scopo di rispondere a una qualche domanda precisa e circostanziata, non a rappresentare l’intero spettro degli effetti di quel farmaco sull’uomo.
I test pre-clinici, ad esempio, servono a stabilire la dose di sicurezza relativa alla tossicità acuta, e lo fanno con un’attendibilità esemplare. Non servono a stabilire la tossicità fetale. Sono attendibili, per ciò che è loro richiesto, e non lo sono per ciò che non è loro richiesto.
D’altra parte, se ci riflette su, l’idea che la SA debba essere attendibile per ogni aspetto della farmacologia (idea sbagliata che le è stata inculcata dagli anti-SA) non sta in piedi: se davvero fosse così (o si facesse finta che sia così), i farmaci dovrebbero passare direttamente dal laboratorio agli scaffali delle farmacie, invece vengono sperimentati sull’uomo.
Questo perché gli effetti a medio-lungo termine – e soprattutto il bilancio rischi/benefici, la principale causa di abbandono delle molecole durante la sperimentazione clinica! – possono essere sperimentati solo sull’uomo. Ed è quello che si fa.
Gli esperimenti su animali servono a rispondere ad altre domande, che precedono la sperimentazione umana. E quegli esperimenti possono essere più o meno attendibili a seconda dei casi, e gli esempi che lei cita sono proprio la dimostrazione che i ricercatori si interrogano sull’efficacia dei cosiddetti “modelli animali” e scartano quelli che non funzionano.
Ma questo glie lo avevo già spiegato!
Il genere di esempi che lei ha copincollato (al netto della sibillinità delle parole usate, sulla quale ci sarebbe veramente tanto da riflettere), sono proprio un secondo punto di contraddizione della propaganda anti-SA: prima si sostiene che i cosiddetti modelli animali non sono validati, poi, per dimostrare che la SA non funziona, si tirano fuori le ricerche fatte per validare questi modelli (in particolare quelle, e solo quelle, che indicano un’inadeguatezza). Insomma, quelle stesse ricerche che dieci secondi prima si era sostenuto sostenuto non esistessero!
Ma è ancora convinto che le fonti cui si è affidato fino ad oggi siano serie, affidabili e, soprattutto, intellettualmente oneste???
Sicuro sicuro scicuro? Neanche un piccolo dubbio?
(sarebbe carino che la smettesse con i copincolla e provasse a esprimere delle idee sue, perché questi copincolla costringono a un grande lavoro extra chiunque abbia la pazienza di cercare di farle capire qualcosa).
Scusi sign.Word, mi spiegherebbe come posso parlare dei bugiardini senza citarli?Se non lo facessi mi direbbe giustamente che argomento per sentito dire o su fonti “animalare” o senza “fonti reali”..Mi faccia capire?! vuole il commentino Twitter da decerebrati? Mi spiace ma io, lavorando in campo giuridico, sono abituata ad argomentare le mie perplessità avendo in mano prove a conferma dei miei dubbi..scusi.deformazione professionale.. Se vuole le rispostine animalare lo dica, capisco che sia più comiche e più facili da trattare ma non fanno per me.Io fin dall’inizio ho parlato di malati umani, perchè è un dramma che mi tocca da vicino e che ha fatto si che passassi anni ad approfondire in quale rete sperimentale si trova lo speranzoso malato UMANO attuale.
Allora dovrò accontentarmi di tirare a indovinare, facendo ipotesi sul modo in cui interpreta i copincolla di frasi sibillinamente estratte dal loro contesto, senza avere informazioni dirette su cosa ne pensa lei esattamente. Farò un ultimo tentativo di chiarire un po’ di punti, sparando nel mucchio, nella speranza di beccarci. Un lavoraccio extra, ma tant’è, bisogna fare con ciò che si ha a disposizione (che è un po’ il leitmotiv della SA, btw).
Sperando che sia chiaro il ruolo della SA nella stima della tossicità acuta, provo a chiarire qual’è la situazione per quanto riguarda il grosso problema della teratogenicità. Scelgo (a caso, non posso fare altro) uno degli esempi da lei copincollati, che ritengo rappresentativo del problema, che quoto, per comodità.
«Il topiramato, al pari di altri farmaci antiepilettici, si e’ dimostrato teratogeno negli animali. Non vi sono studi sull’uso del topiramato in gravidanza. Dall’esperienza post-marketing, sono stati riportati alcuni casi di ipospadia nei bambini maschi esposti al trattamento con topiramato durante la gravidanza, anche in associazione con altri antiepilettici. Non e’ stata riconosciuta una correlazione causale diretta con topiramato.»
Cosa vuol dire esattamente questa frase?
Questo antiepilettico è stato testato su animali gravidi, nei quali si è dimostrato teratogeno. Questo ha fatto sì che, ovviamente, il farmaco non venisse usato sistematicamente su donne incinte. Già questo non è poco, e sarebbe sufficiente a giustificare in questo caso il ricorso alla SA. Tuttavia vi sono stati casi in cui non c’erano alternative alla somministrazione a donne incinte (le crisi epilettiche possono portare all’aborto o anche alla morte), per cui sono arrivati ai servizi di farmacovigilanza (Fase IV del trial di un farmaco) alcune segnalazioni riguardanti possibili malformazioni fetali, anche se apparentemente non gravi. I dati sono troppo scarsi per poter dire qualcosa di ragionevolmente certo, ma sono segnalati, e vengono quindi riportati.
Come si comporterà un medico di fronte a questi dati (sia quelli derivanti dalla SA, sia le poche segnalazioni su uomo)? Un medico farà ricorso a questo farmaco se e solo se non vi sono alternative. Se non vi fossero i dati derivanti dalla SA, il farmaco sarebbe stato prescritto in molti più casi, e forse oggi avremo un nuovo “caso-talidomide”. Per fortuna abbiamo i dati derivanti dalla SA, che ci hanno portato a limitare al minimo i rischi. Senza questi dati, le poche segnalazioni riguardanti i casi di malformazione, e la relativa benignità degli effetti segnalati, probabilmente indurrebbero i medici a prescrivere questo farmaco più spesso di quanto non accada oggi, nelle donne incinte. Invece abbiamo i dati sulla SA, che ci consentono di non sottovalutare quelle segnalazioni apparentemente poco significative, e di evitare quindi rischi inutili. Questo non è poco, ed è tutt’altro che un fallimento della SA: è un successo della stessa.
Tuttavia, nel campo specifico della teratogenicità, l’attendibilità della SA non è certo entusiasmante, soprattutto perché i test di teratogenicità si fanno da tempi relativamente brevi. Con il tempo, e l’accumularsi dei dati, l’attendibilità migliorerà.
Nel frattempo, che facciamo? Rinunciamo a questi dati, rischiando un talidomide-bis, -ter, -quater… oppure ci “accontentiamo” dei dati indiretti che ci arrivano dalla SA, per quanto essi siano meno affidabili di quelli sulla tossicità acuta?
L’attendibilità della SA non è una questione tutto-o-niente, non è nero-o-bianco. È un’infinita serie di sfumature di grigio, molte delle quali sono comunque utili, pur con le loro incertezze (Feynman diceva che se qualcuno è convinto di trovare certezza nella scienza, l’errore è sicuramente suo). Quando invece l’incertezza è troppa – come nel caso dei farmaci ad uso pediatrico – il modello animale non viene preso in considerazione. Noti anche che, se fosse vera l’ipotesi che la SA serve solo come forma di tutela legale, si farebbe un sacco di “SA pediatrica”. Invece praticamente non se ne fa.
Spero che i nostri sforzi siano almeno riusciti a farle intuire l’enorme complessità del ruolo che la SA ricopre nella ricerca biomedica e, mi creda, abbiamo a malapena scalfito la superficie. Non abbiamo neppure cominciato a parlare di ricerca di base. Complessità, quella della ricerca biomedica, che è quanto di più lontano possa esserci dalla visione infantile e distorta propagandata implicitamente dall’ideologia anti-SA (lo straw man argument di cui le ho accennato).
Ma lo straw man argument non è l’unica fallacia logica che deve sforzarsi di scrollarsi di dosso. Un’altra è la tendenza a ragionare di SA in termini di bianco e nero, di tutto o niente. Una vera e propria falsa dicotomia, altro caposaldo della disinformazione anti-SA. L’attendibilità della SA (ma anche della sperimentazione sull’uomo!) è sempre e comunque una sfumatura di grigio. Questo ci offre madre natura, e con questo dobbiamo confrontarci.
Inoltre, dovrebbe anche lavorare su un suo tratto caratteriale – molto diffuso tra coloro che hanno fatto studi giuridici, per ragioni che credo le saranno ovvie. Una persona che ho incrociato tempo fa su FaceBook ha definito questo tratto caratteriale in modo magistrale, ovvero come “la tendenza a discutere per avere ragione, anziché per capire”. Capirà che per chi ha alle spalle studi giuridici si tratta quasi di una necessità professionale. Però questo modo di approcciarsi agli argomenti è l’esatta antitesi del metodo scientifico.
Ma non è tutto. Dovrebbe anche sforzarsi di distinguere tra la ”documentazione” basata su opinioni, e la documentazione (senza virgolette) basata su dati fattuali. Mi
rendo conto che in ambiente giudiziario, e non solo, questi due modi di “dimostrare” tendono troppo spesso ad avere uguale valore. La schizofrenia delle sentenze dei tribunali, anche riguardo al caso Stamina, ne sono la prova. Nella scienza, però (leggi: nella vita reale) contano solo i dati fattuali. Le opinioni non hanno conseguenze meteorologiche. Delle opinioni si può anche ridere, ma non ha senso deridere i dati sperimentali, come ha tentato di fare lei riguardo all’attendibilità della SA nella stima della dose tossica acuta di una molecola. Si rende conto di quanto è sciocco deridere un dato sperimentale? Potrà forse funzionare come espediente retorico in un’aula di tribunale, ma la realtà – qualunque cosa essa sia – se ne frega dei tribunali. Se ne frega di quello che pensiamo noi. La realtà non ha pietà di nessuno. Deve sforzarsi di imparare a distinguere tra dati e opinioni, altrimenti continuerà a scambiare le opinioni degli ideologi per “legittime dimostrazioni”, copincollandole magari a sproposito. Se non si sforza di scrollarsi di dosso anche questo problema, non approderà a nulla di sensato.
E adesso la pianto veramente lì.
Perché cercare di spiegare le cose a chi si spiega a suon di copiaincolla è come fare il tiro al piattello con gli occhi bendati.
Perché stavamo cercando di tirar fuori qualche dato concreto riguardo al Metodo Stamina, e invece siamo finiti a discettare di protocolli di sperimentazione. Che, per carità, c’entrano, ma solo fino a un certo punto.
Soprattutto, perché è mia personale convinzione (non solo mia, per la verità, ma potrei comunque sbagliare), che tutto ciò sia una fatica inutile, perché dall’altra parte non sono riuscito a scorgere nemmeno un briciolo di volontà di capire. Il famoso “discutere per avere ragione”. E come dice un vecchio proverbio cinese, (con la consueta enfasi sul rappresentare l’apprendimento sempre e comunque come rapporto interpersonale):
«un maestro può aprire una porta, ma tu devi attraversarla da solo».
@ marmanu. Non ho risposto prima anche perché ho visto l’ intervento di WordsOutsideReality che mi sento di sottoscrivere pienamente.
Posso aggiungere solo una cosa, dalla mia pratica clinica quotidiana.
Studi in doppio cieco si fanno -come detto sopra- con farmaco noto (p. es. per avere un’ efficacia del 60%) più farmaco nuovo (nell’ipotesi che possa avere un effetto additivo) vs. farmaco noto + placebo. Oppure: farmaco in studio a dosaggi diversi (in cieco) per valutare risposta ed effetti collaterali e quindi dose ideale. Una sperimentazione interessante (che conosco bene perché ci partecipo anche io) è stata quella sul Trastuzumab (Herceptin), anticorpo monoclonale contro un recettore presente in gran quantità in alcuni tumori della mammella. In donne operate e senza malattia (quindi guarite) è stata fatta la chemioterapia adiuvante (quella per prevenire le recidive) standard per 3 mesi, poi c’è stat la randomizzazione in doppio cieco a Trastuzumab contro Placebo. Chi prendeva il placebo faceva quello che tutte le donne prima (e quelle non partecipanti alla sperimentazione) facevano, quelle con Herceptin avevano un farmaco in più potenzialmente utile ma anche con un noto rischio di tossicità cardiaca. L’arruolamento doveva durare 4 anni, e i risultati sarebbero arrivati dopo altri 5 anni (bisognava verificare quante donne in ognuno dei due gruppi avrebbero avuto una recidiva di tumore entro 5 anni), ma il follow-up previsto è di 10 anni (ancora in corso). Però in questi studi i dati clinici dei pazienti vengono inviati alla casa farmaceutica (che ha i codici di randomizzazione, cioè sa chi fa cosa) man mano che vengono raccolti. Dopo due anni l’analisi dei dati già raccolti ha dimostrato che chi non faceva l’ Herceptin aveva un rischio di recidiva di tumore dimezzato (cioè 50% in meno) rispetto a quelli che facevano il placebo, con un rischio di tossicità cardiaca del 4% in più, per cui è stato considerato non etico continuare la randomizzazione, sono stati aperti tutti i codici e a chi stava prendendo il placebo è stato offerto di passare al trattamento. Se invece avessero osservato una riduzione delle recidive del 10% ma un eccesso di disfunzione cardiaca del 20% in chi faceva l’ Herceptin avrebbero bloccato lo studio e smesso di dare l’ Herceptin. Al momento dell’ arruolamento, n essuno poteva sapere quale dei due gruppi avrebbe avuto un vantaggio. Chiaro il concetto?
La invito anche a leggere questo bell’ intervento (e si legga anche i vatri link, incluso lo scambio di lettere tra Vannoni e i genitori dei bambini con SMA1.
http://medbunker.blogspot.it/2013/09/staminali-vannoni-capitolo-chiuso-ora.html
Ora: l’associazione Luca Coscioni ha lanciato una raccolta di firme perché il famoso metodo sia reso pubblico, l’ associazione dei malati di distrofia muscolare pure, l’associazione genitori SMA1 è amareggiata per la mancanza di chiarezza e collaborazione di Stamina… che siano anche loro al soldo di Big Pharma?
ho sbagliato a scrivere: il testo esatto è ” Chi FACEVA l’ Herceptin aveva un rischio di recidiva di tumore dimezzato (cioè 50% in meno) rispetto a quelli che facevano il placebo… “
Nel gioco delle 3 carte si è scordata di cercare di mettere una toppa alla questione “volontari SANI”…cmq anche se non sono soddisfatta delle risposte che ha dato vorrei porle poi altre domande:
1)Lei dice:Studi in doppio cieco si fanno con farmaco noto più farmaco nuovo vs. farmaco noto + placebo,DOMANDA se fosse cosi come dice e non fosse come temo (cioè placebo = NULLA=speranza del “malato cavia” giù nel..secchio) come farebbe a distinguere l’effetto reale del farmaco nuovo DA SOLO?
2)Lei parla di “arruolamento”..ci dice come avviene?Vorrei sapere dove sta la differenza con l’arruolamento fatto da Vannoni..anzi, come dicevo almeno lui non sperimenta sui sani..
3) Lei, nel suo esempio, parla di rischio cardiaco..non è forse la prova che TUTTE le sperimentazioni cliniche prevedono che la cavia umana possa andare incontro ad un rischio (più o meno grave),anzi, idem x l’assunzione di qualsiasi farmaco attualmente in commercio….ma ciò (gravi rischi ed effetti collaterali) sono giustificati per tutti /aziende farmaceutiche, ricercatori, ecc)tranne che per il metodo Staminal??
4) Lei dice”in questi studi i dati clinici dei pazienti vengono inviati alla casa farmaceutica (che ha i codici di randomizzazione, cioè sa chi fa cosa)”..questa è la setsdsa trasparenza richiesta a Vannoni o sono 2 pesi e 2 misure, dii nuovo?e poi, nel suo commento, si scorda di dire che SOLO la casa farmaceutica mette insieme tutti i tasselli..mi domando, li assemblerà bene o magari ci mette qualche ritocchino per non perdere un sacco di soldi?E poi..quando iniziano ad esserci troppi morti il farmaco taldeitali viene ritirato alla chetichella?(cronaca sanitaria)..Inoltre sbaglio o è prevista la segretezza della procedura?Sbaglio o il ricercatore che inocula la sostanza da testare non sa bene se sta dando quella o il placebo?E quindi come fa a leggere i sintomi del paziente trattato?..scusi ma io in questo standard Modus operandi legale,ci vedo molte somiglianze proprio con le procedure per cui volete mettere Vannoni in croce..
5) sottoscrive anche la percentuale del “cientopeciento” ?e sul glissare le citazioni di suoi illustri colleghi anche stranieri che ho messo in precedenza?
gli articoli e le testimonianze parlano da sole… anche se una mente acuta non avrebbe avuto bisogno di queste ulteriori prove.
http://www.ilfattoquotidiano.it/2014/01/14/stamina-la-procura-di-torino-valuta-larresto-di-vannoni/842343/
http://www.ilfattoquotidiano.it/2014/01/14/bianco-cattaneo-e-de-luca-premiati-gli-scienziati-italiani-contro-stamina/842822/
http://www.ilfattoquotidiano.it/2013/07/02/staminali-nature-contro-stamina-presentata-documentazione-fallace/
http://www.ilfattoquotidiano.it/2013/04/10/cellule-staminali-premio-nobel-yamanaka-no-prove-efficacia-metodo-stamina/558462/
1) Nella fase farmaco vecchio + farmaco nuovo/placebo si trattano malati, senza negare a nessuno una terapia. Se si vuole testare il farmaco da solo in un malato si confronta con un farmaco di cui è già nota l’efficacia e si valuta se è inferiore/non inferiore/superiore. Nei casi di mancanza di altra terapia notoriamente efficace (per esempio, in caso di tumore resistente a tutte le terapie già note) è possibile testare un farmaco nuovo, ma vengono stabiliti a priori quali sono i parametri di risposta e vengono verificati frequentemente (nel campo dei tumori de esserci una lesione misurabile, e si valuta se la lesione si riduce, rimane invariata o si riduce, per esempio). Nello studio HERA che ho citato il farmaco nuovo veniva dato a donne NON MALATE, solo per vedere se preveniva le recidive, dopo la terapia standard che si faceva già prima.. Le donne che prendevano il placebo semplicemente facevano quello che si faceva in passato.
2) Lo studio clinico deve essere prima approvato da un comitato etico, che valuta il razionale del trattamento (come agisce il farmaco e perché si pensa che potrebbe essere utile in quella patologia?), gli studi pre-clinici (in vitro e nell’animale, sia di efficacia che di tossicologia), una sintesi degli studi già pubblicati, criteri di inclusione e di esclusione (p. es entrano nello studio i paz. che hanno la patologia tale, ma sono esclusi quelli che hanno 75 anni, che hanno una malattia di cuore, che hanno un’ insufficienza renale….), il metodo di valutazione dei risultati (incluse le schede di raccolta dei dati) e la dimensione del campione (se mi aspetto che il farmaco sia efficace nel 90% dei casi avrò bisogno di una casistica minore che se mi aspetto che funzioni nel 70% dei casi), anche considerando quanto può sbagliare il mio metodo di valutazione. Il Comitato Etico (CE) valuta anche la qualità dell’ informazione che verrà fornita al paziente (cioè: bisogna consegnare anche la scheda informativa che spiega razionale dello studio, possibili vantaggi, possibili rischi, a quali esami dovrà sottoporsi ecc. In genere si tratta di due o più pagine), come è strutturato il foglio del consenso informato che verrà firmato dal paziente e altre cose. Se c’è una possibilità che il paziente corra dei rischi, viene stipulata un’ assicurazione ad hoc. Passato lo scoglio del CE (che è molto duro), quando un paziente è “arruolabile” (cioè rientra nei criteri di inclusione e non in quelli di esclusione) gli si spiega in cosa consiste lo studio, gli si fornisce la documentazione scritta, oltre a spiegargli a voce pro e contro della sperimentazione. Dopo aver ricevuto le informazioni, il paziente -se decide di partecipare- firma il foglio del consenso informato. Se non vuole, verrà curato secondo pratica standard. Se accetta, e lo studio è randomizzato, i suoi dati vengono mandati al centro di randomizzazione che lo arruolerà in un braccio di trattamento o nell’altro, con un sistema che garantisce che nei due bracci finiscano pazienti abbastanza simili per sesso, età, malattia ecc. Se durante lo studio il malato ci ripensa, è libero di uscirne e verrà curato secondo pratica standard. Le schede di valutazione dei risultati e degli esami che possono rivelare eventuali effetti collaterali vengono compilate a ogni controllo, verificate periodicamente da un “data monitor” della casa farmaceutica che verifica che siano complete in ogni dettaglio.
3) negli studi pre-clinici si valuta la possibilità di effetti collaterali dannosi. La scelta di passare alla sperimentazione umana si fa se c’è una ragionevole probabilità che i vantaggi siano superiori ai danni.
Per registrare un nuovo farmaco la casa farmaceutica deve consegnare agli organismi regolatori (FDA negli USA, EMEA in Europa, e -dopo l’approvazione dell’ EMEA- anche all’ AIFA in Italia e ai corrispondenti organi negli altri stati) tutta l documentazione della sperimentazione.
Certamente poi, nell’applicazione in clinica, possono saltare fuori atri effetti collaterali non previsti. Ma questo succede di solito non durante la fase sperimentale dello studio randomizzato (dal quale in genere vengono esclusi i pazienti con altre patologie) ma dopo l’immissione in commercio, quando il farmaco viene dato anche a pazienti più “fragili”. Chiunque nota un possibile effetto tossico ha l’obbligo di comunicarli all’ AIFA, che poi lo comunica anche all’ EMEA (in europa); negli USA la comunicazione va alla FDA. Se le agenzie ricevono un certo numero di segnalazioni fanno un WARNING, cioè comunicano a tutti i medici potenzialmente prescrittori che ci sono state queste segnalazioni, così tutti stanno più attenti e le segnalazioni possono aumentare (se l’effetto collaterale è frequente).
4) la parte di dati di proprietà della casa farmaceutica è effettivamente una nota dolente, perché gli studi post registrazione possono rivelare cose nuove che la casa farmaceutica non ha interesse a divulgare. Per questo motivo è in corso una battaglia da parte di associazioni mediche, del British Medical Journal e di molti medici (io ho sottoscritto la petizione) perché questi dati vengano resi accessibili a tutti.
Quello che Vannoni NON ha fatto è: a) fare una valutazione in vitro di quante cellule staminali si creano con il suo metodo; b) fare un test sui topi (non -come dice lui- con staminali umane ma con staminali di topo preparate con il suo metodo) per verificare che l’iniezione nel midollo non abbia effetti collaterali e queste cellule attecchiscano; c) fare delle preparazioni di staminali umane e verificare dopo coltura con il suo metodo se si differenziano in neuroni e solo in neuroni, quante staminali si formano, se queste cellule hanno la tendenza a degenerare a tumore, se producono sostanze tossiche, se il terreno di coltura è libero da inquinanti ecc. ecc.; d) prima di passare all’ uso nell’ uomo prendere contatti con una struttura pubblica o accreditata, presentare i suoi dati a un Comitato Etico che valutasse le cose di cui sopra, oltre al fatto che le cellule venissero preparate in un ambiente idoneo con rispetto di tutte le regole di sterilità (penso a quello che faceva a Torino); e) controllare ogni 2-3 mesi al massimo come stavano i pazienti trattati, raccogliere dati verificabili (elettromiografie, filmati ) e compilare schede precise con tutti i dati per tutti i pazienti, in modo da poter poi stabilire quanti pazienti sono migliorati, quanti sono peggiorati, quanti non hanno avuto cambiamenti.
“NON malate”..punto dolente:,se il giuramento di Ippocrate dice 1) NON NUOCERE perchè uso persone sane che , come effetto collaterale, potrebbero perdere il loro stato di salute?
La sua spiegazione magari può essere attinente al suo caso ma la normativa di riferimento lascia delle libertà che mi turbano (anche perchè, in ogni ambito, se si è onesti, la libertà va bene, se si è disonesti, non tanto), e non solo io sono perplessa visto che ci sono atti di convegni che parlano proprio di queste criticità (glieli copierei e incollerei volentieri ma mi si è fatto notare che non è cosa gradita)..La stessa perplessità l’ ho provata ficcanasando tra i membri di alcuni comitati etici..che (IN TEORIA) dovrebbero essere super partes e svincolati da altri interessi..
X ciò che riguarda i bugiardini , se li ha letti TUTTI, il quadro di INSIEME che volevo evidenziare è un altro rispetto a quello che lei scrive e cioè , leggendoli tutti insieme, dal CONFRONTO emerge che: se la molecola X (es CYTOTEC, RETROVIR,..) fa male agli animali si continua nella sperimentazione, se non fa male si continua, se in una specie fa male e in un altra no si continua lo stesso, quindi visto che non funziona da filtro, a cosa serve? Mi viene da pensare che serva o, come scrive REISS, per trovare la specie adatta tra le tante che la natura ci offre e avere anche un salvacondotto legale nel caso le cose dovessero mettersi male in humana, oppure anche per “facilitare” la firma del consenso informato nei pazienti di trial clinici di fase1(cioè il primo step umano dopo l’animale)..anche per questo continuo a pensare che Vannoni abbia almeno 2 meriti:non aver sprecato tempo e soldi sugli animali che non hanno malattie rare (cosi come non ce le ho io o lei nè il topo che si invoca tanto), e aver sperimentato solo su malati(che si erano offerti) e non su sani che hanno solo da perderci…(e per la questione sterilità degli ambienti sanitari..non è sicuramente colpa di vannoni se negli ospedali pubblici la sterilità e una ambizione fantascientifica)
La ringrazio per la franchezza del punto 4 e le chiedo se può allegarmi il link dove si può leggere la petizione di cui parla.
Non malate significa che fanno una terapia cosiddetta adiuvante, che serve a prevenire la recidiva della malattia. Dopo l’intervento chirurgico non c’è più malattia (nel senso di malattia evidenziabile), ma si sa che alcuni tumori ricompaiono in una certa percentuale di pazienti entro un certo numero di anni, perché evidentemente qualche cellula può essere migrata prima dell’ intervento chirurgico (infatti si asportano i linfonodi che sono il primo filtro). Per questo vengono fatte DI ROUTINE delle chemioterapie che hanno lo scopo di sterilizzare l’organismo da eventuali micrometastasi. Sono cure che vengono OFFERTE, non imposte. E’ come comprare una costosa porta blindata per difendermi dai ladri. Affronto una spesa subito (magari inutile perché forse i ladri non verranno mai), ma ho una protezione in più nel caso che venissero a svaligiarmi la casa (e in tal caso ci avrei guadagnato).
Quanto ai foglietti illustrativi, lei ha citato i problemi in gravidanza. Dunque se un farmaco ha effetti dannosi sul topo in gravidanza perché si dovrebbe bloccare del tutto? Semplicemente, si avverte che in gravidanza non bisogna usarlo. Se una molecola a dosi elevatissime provoca danni, ma la dose terapeutica è 100 volte più bassa, perché si dovrebbe interrompere la sperimentazione?. Guardi che TUTTO in dosi eccessive può essere tossico! La vitamina D che è servita a sconfiggere il rachitismo, in dosi elevate fa male. Infatti gli eschimesi che mangiano il fegato dell’ orso polare si possono ammalare. Ma se uno pretende le dosi terapeutiche non succede niente.
Quello che si contesta a Vannoni non è di non aver testato il suo metodo sui topi ammalati, ma di NON AVER VERIFICATO SUI TOPI -PRIMA DI SPERIMENTARE SULL’ UOMO- SE IL SUO METODO PRODUCE CELLULE STAMINALI, SE L’ INIEZIONE NEL MIDOLLO E’ SICURA (NON CAUSA REAZIONI INFIAMMATORIE, PER ES.) SE QUESTE CELLULE ATTECCHISCONO, SE SI TARSFORMANO SOLO IN NEURONI E NON INVECE IN OSSO… ECC. ECC.
VANNONI HA SALTATO COMPLETAMENTE LA FASE DI SPERIMENTAZIONE DI BASE IN CUI SI DIMOSTRA CHE IL METODO PUO’ FUNZIONARE E CHE NON HA EFFETTI COLLATERALI GRAVI.
Quanto all’ ultima affermazione “(e per la questione sterilità degli ambienti sanitari..non è sicuramente colpa di vannoni se negli ospedali pubblici la sterilità e una ambizione fantascientifica)” legga bene: avevo specificato:(penso a quello che faceva a Torino). E aggiungo a S. Marino. Lui ha cominciato a iniettare staminali in un locale sotterraneo a Torino, poi in un centro estetico a S. Marino.
Il problema poi non è che negli ospedali pubblici la sterilità sia un’ ambizione fantascientifica. Semplicemente, per trattare staminali è necessario un laboratorio con particolari caratteristiche di sicurezza, superiori a quelle di altri laboratori. Al Burlo a Trieste, quando il giudice ha imposto di fare i trattamenti, non hanno fatto lavorare le cellule da loro perché il laboratorio in cui si preparano le cellule per i trapianti di midollo emopoietico (che a Trieste si fanno) non ha le caratteristiche sufficienti per lavorare cellule staminali mesenchimali. Quindi hanno chiesto che le cellule venissero prodotte in uno dei 13 laboratori autorizzati che ci sono in italia. Nel mio ospedale fanno da anni trapianti di midollo, e vorrebbero fare anche trapianti di staminali; per questo stanno preparando un laboratorio ad hoc a norma di legge. A Brescia, da quel che so, usavano il laboratorio dove si preparano i trapianti di midollo.
Vede, lei leggiucchi qua e là delle cose, estrapola e crede di aver capito tutto… le cose sono molto molto più complicate di quanto lei immagina (e anche più di quello che immaginavo io, prima di parlare con i colleghi che si occupano di questo e di leggere la letteratura scientifica)
La campagna per la diffusioni dei dati delle pubblicazioni è qui.
http://www.cochrane.it/it/una-ricerca-trasparente
Vorrei chiarire: non credo assolutamente che le case farmaceutiche siano enti di beneficenza, sono convinta che in certi casi giochino sporco “pompando” certe patologie o certi rischi per aumentare le vendite (la storia dell’ influenza aviaria è un ottimo esempio), e che -potendo- tendano a nascondere quello che non fa loro comodo. Ma non credo assolutamente che si scomodino a fare la guerra a due illustri sconosciuti (all’estero) come Vannoni e Andolina per proteggere non si sa quali interessi (visto che non ci sono farmaci per queste malattie rare). C’è tanta tuffa anche nella letteratura scientifica, ogni tanto qualcuno viene preso con le mani nella marmellata e studi già pubblicati vengono ritirati. Ed è ben vero che tra gli esperti in un campo ci sono rivalità e sgambetti fatti dai più potenti a quelli meno appoggiati politicamente (lo so anche per esperienza personale). Peraltro, come ha ammesso Andolina, a Brescia non ci sono arrivati avendo dimostrato la validità del loro metodo, ma per amicizie personali (l’ allievo di andolina, Porta) e appoggi politici in Regione.
E tutto il marcio che c’è nella medicina non giustifica il comportamento di una persona che da almeno 5 anni esegue trattamenti di cui non si sa nulla, che per almeno 3 anni li ha fatti fare in condizioni igieniche non adeguate, che si è spacciato per “neuroscienziato”, che ha sfruttato la disperazione dei malati incoraggiandoli a scendere in piazza per ottenere le autorizzazioni che tutti i medici seri si guadagnano dimostrando la validità del loro lavoro (in pratica: ha saltato la fila), che dice tutto e il contrario di tutto.
L’ ultima: ha messo sul suo profilo FB il video della bambina Nicole (tra l’altro visitata da lui, non da un medico), riconoscibilissima. Cosa vietata dalla legge sulla privacy (pensi che il mio ospedale mi ha negato il permesso di far analizzare da un collega di altro ospedale le immagini anonime di alcune ecografie se non ottengo il consenso dei pazienti!). Adesso che è stato -giustamente- denunciato dice che il video era stato pubblicato dal comitato pro-stamina. Ma il video lo aveva girato lui! Chi può averlo dato al comitato?. E lo ha messo sul suo profilo FB. Come Scaiola? “Non sapevo che qualcun altro avesse pagato per me l’appartamento”!
Grazie per il link…per la questione dei sani intenedevo i SANI del mio primo commento..ma vabbè..capisco che sia difficile parlarne…
per Vannoni non intendo santificare nessuno ma sia nei mass media, sia nelle varie interviste mi sambra impossibile che si concentri tutto su di lui..nel senso che è come se ci si dovesse occupare di Riina, del mostro di Firenze e di un piccolo caso, e si parlasse solo di quest’ultimo..per la questione topi , se non mi è consentito copiare e incollare documenti , testi di conferenze e dichiarazioni di scienziati e ricercatori non so cosa dirle oltre a quello che ho già detto e che già fa evincere chiaramente cosa intendo..
Volevo, a tal proposito, citare uno studio famoso che dimostra quanto i ricercatori abbiano “i topi davanti agli occhi” anzichè i malati..ma senza farvelo leggere da voi non posso rendere bene l’idea .
E, quanto alle citazioni dei foglietti informativi: appunto, qualsiasi effetto collaterale osservato, per quanto raramente, viene segnalato. Quasi tutti i farmaci sono sconsigliati in gravidanza perché appunto non sarebbe etico fare uno studio di teratogenicità nella donna. Gli studi di teragenicità vengono fatti nell’animale e -se il farmaco appare teratogeno- viene controindicato in gravidanza; se non è teratogeno -siccome non si ha la certezza che non lo sia neanche per la donna- viene sconsigliato. Con l’uso più diffuso dopo l’ introduzione in commercio, capita che donne incinte lo assumano lo stesso (magari perché non sanno di essere incinte, oppure perché sottovalutano il rischio); questo può aiutare a capire se il farmaco è davvero pericoloso o no.
Per fare un paragone: nessuno si sognerebbe mai di sottoporre a radiazioni un uomo solo per vedere quello che succede, ma ci sono interessantissimi studi sui sopravvissuti ai bombardamenti atomici di Hiroshima e Nagasaki, che ci dicono moltissimo sugli affetti di vari carichi di radiazioni, anche in rapporto all’ età di esposizione, come verranno fatti sicuramente molti studi sugli abitanti di chernobyl.
@ marmanu: “per Vannoni non intendo santificare nessuno ma sia nei mass media, sia nelle varie interviste mi sambra impossibile che si concentri tutto su di lui..nel senso che è come se ci si dovesse occupare di Riina, del mostro di Firenze e di un piccolo caso, e si parlasse solo di quest’ultimo..”.
Innazitutto, originariamente questo blog parlava di Stamina, quindi di Vannoni, non della sperimentazione animale
Poi, Vannoni ha venduto un metodo che non è stato validati scientificamente, e ogni volta che gli si contesta qualcosa fa il gioco delle tre carte e cambia argomento.
La rivista Nature scrive due editoriali di critica a come si è svolta questa faccenda? Lui accusa Nature di essere un giornalucolo fazioso.
Poi -quando uno scienziato di fama critica pubblicamente la politica editoriale di Nature- lo sbandiera come un suo supporter.
Mettendogli in bocca parole che non ha mai detto.
Questo è lo stile (o il “metodo”) Vannoni, e per questo non mi fiderei di lui neanche se a ferragosto mi dicesse che fa caldo.
http://tv.ilfattoquotidiano.it/2014/01/19/stamina-nobel-schekman-non-sostengo-quel-metodo-si-opera-unoperazione-criminale/261669/
le ho solo scritto una mia opinione: uno dei meriti di Vannoni e di non aver sprecato soldi e tempo con animali..quello che lei chiama validazione ..e che io chiamo (in)validazione perchè la validità dei test animali non è mai stata dimostrata.. fonte FDA statunitense sulla tossicologia ha affermato nel 1998 che “La maggior parte dei test sugli animali che accettiamo non sono mai stati validati. (infatti negli Usa non valgono nemmeno come prova in Tribunale)
cmq ha toccato un altro discorso molto interessante: quello delle riviste e delle pubblicazioni..e non è solo Vannoni che dice che sia un altro punto dolente…
Crolla il valore scientifico del topo come modello delle malattie letali nell’uomo
(Mice Fall Short as Test Subjects for Human’Deadly Ills)
Per decenni, i topi sono stati la specie più utilizzata nello studio delle malattie umane. Ma adesso i ricercatori hanno ottenuto la prova che il modello murino sia stato totalmente fuorviante per almeno 3 diversi tipi di patologie mortali (sepsi, traumi e ustioni). Di conseguenza, essi affermano, che anni di lavoro e miliardi di dollari sono stati sprecati seguendo false piste.
Ciò non significa che il topo sia un modello inutile per tutte le malattie umane. Tuttavia, essi sollevano interrogativi su patologie come quelle che riguardano il sistema immunitario, inclusi cancro e disturbi cardiaci.
“Il nostro articolo apre la possibilità ad una situazione parallela di essere presente”, dice il Dr. H. Shaw Warren, un ricercatore sulla sepsi all’Ospedale Generale del Massachusetts e uno degli autori principali del nuovo studio.
L’articolo, pubblicato lunedì in “Proceedings of the National Academy of Sciences”, aiuta a spiegare perché sono falliti tutti i circa 150 farmaci, testati con enorme dispendio su pazienti affetti da sepsi. Tutti i test farmacologici si basavano sullo studio dei topi. E adesso viene dimostrato che i topi possono avere qualcosa che assomiglia alla sepsi negli uomini, ma in realtà è una condizione molto diversa da quella umana.
Esperti medici non legati a questo studio hanno detto che i risultati dovrebbero cambiare il corso della ricerca a livello mondiale per tale fatale e frustrante patologia. La sepsi, una reazione potenzialmente mortale che avviene quando il corpo prova a lottare contro un’infezione, colpisce 750 000 pazienti all’anno negli USA, uccide da un quarto alla metà di essi e costa alla nazione 17 miliardi di dollari all’anno. E’ la principale causa di morte nelle unità di terapia intensiva.
“Questo è un cambiamento rivoluzionario”, dice il Dr. Mitchell Fink, un esperto della sepsi dell’Università della California di Los Angeles, riguardo al nuovo studio.
“E’ strabiliante”, dice il Dr. Richard Wenzel, ex direttore del dipartimento di medicina interna alla Virginia Commonwealth University e già redattore del ‘New England Journal of Medicine’. “Hanno assolutamente ragione”.
Risposte immunitarie potenzialmente fatali avvengono quando il sistema immunitario di una persona iperreagisce a ciò che percepisce come un segnale di pericolo, incluse molecole tossiche da batteri, virus, funghi o proteine rilasciate da cellule danneggiate da traumi o ustioni, dice il Dr. Clifford S. Deautschman, che dirige le ricerche sulla sepsi all’Università della Pennsylvania e non ha fatto parte dello studio.
Il sistema immunitario accelerato rilascia le sue proteine in quantità talmente elevate che i capillari iniziano a perdere sangue. La perdita diventa eccessiva, e il siero fuoriesce dai piccoli vasi sanguigni. La pressione sanguigna cala, e gli organi vitali non ricevono più sangue sufficiente. Nonostante gli sforzi, i medici e gli infermieri in un reparto di terapia intensiva o pronto soccorso possono non essere in grado di fronteggiare queste perdite, fermare l’infezione e il danno tissutale Successivamente vi è il collasso degli organi vitali.
Il nuovo studio, che è durato 10 anni e ha coinvolto 39 ricercatori in tutto il Paese, è iniziato studiando i globuli bianchi di centinaia di pazienti con gravi ustioni, traumi o sepsi, per vedere quali geni venivano usati dai globuli bianchi nel rispondere a questi segnali di pericolo.
I ricercatori hanno trovato alcune informazioni interessanti e accumulato un grande numero di dati, rigorosamente raccolti, che dovrebbero contribuire a far progredire il settore, ha detto Ronald W. Davis, esperto di genomica presso la Stanford University e autore principale del nuovo studio. Alcuni dati sembravano consentire la previsione di chi sarebbe sopravvissuto e chi sarebbe finito in terapia intensiva, aggrappandosi alla vita e, spesso, morendo.
Il gruppo aveva cercato di pubblicare le sue scoperte in diversi giornali. Un’obiezione, afferma il dottor Davis, era stata che i ricercatori non avevano dimostrato come i topi fornissero la stessa risposta genica.
“Erano così abituati a fare studi sui topi che per loro era quello il solo modo di convalidare le cose”, ha detto. “Hanno la cura dei topi talmente radicata che dimenticano che noi stiamo, invece, cercando di curare gli esseri umani.”
“Questo ci ha fatto pensare”, ha continuato. «Lo stesso avviene nei topi, oppure no?”
Il gruppo decise di indagare, aspettandosi di trovare alcune somiglianze. Ma quando i dati furono analizzati, non ve ne era alcuna.
“Eravamo proprio spiazzati” ha detto il dr.Davis.
I fallimenti dei farmaci divennero chiari. Ad esempio, un gene poteva essere attivato spesso nei topi, mentre il gene equivalente veniva soppresso negli esseri umani. Una sostanza che agiva nei topi disattivando un gene poteva avere una risposta letale nell’uomo.
Ancora più sorprendente, ha affermato il dr Warren, è che condizioni diverse nei topi – ustioni, traumi, sepsi – non creavano la stessa risposta. In ognuna di queste condizioni entravano in azione gruppi di geni diversi, mentre negli esseri umani geni equivalenti vengono utilizzati in tutte e tre le condizioni. Questo significa, ha detto il dr Warren, che se i ricercatori possono trovare un farmaco che funziona per una di quelle condizioni nell’uomo, potrebbe funzionare per tutte e tre.
I ricercatori hanno provato per più di un anno a pubblicare il loro studio, che ha dimostrato non esserci alcuna relazione tra le risposte genetiche dei topi e quelle degli esseri umani. L’hanno presentato a Science e Nature, nella speranza di raggiungere un vasto pubblico, ma entrambi i giornali lo hanno rifiutato.
Science e Nature hanno dichiarato che la loro politica è di non fare commenti su di un documento rifiutato, e nemmeno di far sapere se è stato presentato. Ma, Pinholster Ginger di Science ha dichiarato: la rivista accetta solo circa il 7 per cento dei circa 13.000 studi presentati ogni anno, quindi non è raro che uno studio debba girare a lungo.
Inoltre, il dr Davis ha detto, i revisori non avevano evidenziato errori scientifici. Invece, ha dichiarato, la risposta più comune è stata “Deve essere sbagliato. Non so il motivo per cui è sbagliato, ma deve essere sbagliato.”
I ricercatori si volsero, dunque, verso Proceeding of the National Academy of Sciences. In qualità di membro dell’accademia, il dottor Davis poteva suggerire i recensori per il suo studio e propose i ricercatori che pensava avrebbero dato al lavoro la giusta attenzione. “Se a loro non piace, voglio sapere perché”, ha detto. I revisori hanno consigliato la pubblicazione e il comitato di redazione della rivista, che valuta in modo indipendente gli studi, ha concordato.
Alcuni ricercatori, leggendo lo studio oggi, dicono che sono stupefatti, allo stesso modo i cui i ricercatori lo furono quando videro i dati.
“Quando ho letto lo studio, sono rimasto sbalordito da quanto i dati provenienti dai topi siano sbagliati,” ha detto il dott. Fink. “E ‘davvero incredibile – non vi è alcuna correlazione. Questi dati sono così convincenti e così consistenti che penso che gli enti di finanziamento ne stiano prendendo nota. “Fino ad ora, ha detto,” per ottenere i finanziamenti, si doveva proporre esperimenti che utilizzavano il modello animale.”
Eppure c’era sempre stato un indizio importante che i topi non potevano davvero imitare gli esseri umani in questo ambito: è molto difficile uccidere un topo con una infezione batterica. I topi hanno bisogno di un milione di volte più batteri nel sangue rispetto a quelli che uccidono una persona.
“I topi possono mangiare spazzatura e cibo che è in giro ed è marcio,” ha detto il Dr. Davis. “Gli esseri umani non possono farlo. Siamo troppo sensibili “.
I ricercatori hanno detto che se riuscissero a capire cosa rende i topi tanto resistenti, potrebbero forse trovare il modo di rendere le persone resistenti.
“Questo è un documento molto importante”, ha dichiarato il Dr. Richard Hotchkiss, un studioso di sepsi alla Washington University che non ha partecipato allo studio. “Esso dice con forza – di andare dai pazienti e prendere le loro cellule. Prendere i loro tessuti ogni volta che si può. Prendere le cellule dalle vie respiratorie. ”
“Per capire la sepsi, si devono studiare i pazienti”, ha detto.
Questo studio è stato revisionato
Correzione: 11 febbraio 2013
Una precedente versione di questo articolo ha errato nell’indicare la posizione del Dr Wenzel. Egli è stato presidente del Dipartimento di Medicina Interna della Virginia Commonwealth University. Attualmente non ne è il presidente.
E, per favore, invece che scrivere interminabili copia-incolla di articoli tradotti, metta il link al riferimento bibliografico originale. Frasi estrapolate possono dire il contrario di quel che intendeva l’autore. Bisogna leggere l’articolo e capire. Io faccio così.
siamo alle solite, lei legge UN articolo (probabilmente pescato in qualche gruppo contrario alla sperimentazione animale) e lo utilizza per giustificare una cosa che non c’entra assolutamente niente.
1) Che un farmaco che funziona nel topo possa non funzionare nell’ uomo perché il sistema immunitario è diverso o per altri motivi (soprattutto per differenze nel metabolismo) è ovvio e risaputo. Ed è il motivo per cui agli studi animali SEGUONO gli studi sugli umani. Ma non significa che sia giusto saltare a piè pari questa fase. Perché se il farmaco non funziona NEMMENO nel topo non ha senso provarlo nell’ uomo.
2) ogni nuova terapia deve essere provata prima nelle condizioni in cui ci siano meno variabili possibili aggiunte alla risposta attesa e la risposta possa essere misurata. Cioè, in un nuovo antibiotico (esempio semplice), verificare quante e quali specie batteriche uccide o inibisce in vitro. Sistema semplice, dove ci sono solo batteri, terreno do coltura e antibiotico. POI, se qualcosa sembra promettente perché in vitro funziona, si prova nell’ animale (sistema più complesso) e magari si scopre che l’antibiotico in vivo non funziona molto bene. Allora si cerca di capire dov’è il problema, misurando le concentrazioni nei vari tessuti. Così si capisce se viene mal assorbito, inattivato o altro. Poi si verifica se provoca problemi nell’organismo intero. Solo se nell’ animale il farmaco funziona, non è tossico ecc. si passa all’uomo. Dove magari salta fuori che c’è un problema diverso e allora si butta tutto a mare. Oppure si scopre che in certe persone e funziona e in altre no, e allora si cerca di capire perché e come individuare a priori i responders e dare solo a loro il farmaco. Sistema molto costoso in tempo e soldi, ma il migliore possibile al momento. Che fa sì che solo il 10% dei farmaci valutati in ricerca arrivi alla fine all’ uomo. Saltando i primi due passaggi, si rischia di dare una sostanza inefficace e magari tossica a degli uomini. Lei sarebbe d’ accordo nel provare direttamente nell’ uomo una sostanza che ha il 90% di probabilità di essere inutile e/o dannosa?. Consideri che -già con tutto questo sistema di preselezione- per validare il farmaco per uso umano sono necessari migliaia di pazienti da curare.
3) Vannoni e co. non hanno fatto nemmeno la cosa più semplice ed economica: dimostrare quante cellule staminali trattate con il loro sistema si differenziano in neuroni prima di essere iniettate. E non hanno fatto neanche lo sforzo di tenere un data-base dei pazienti trattati (visto che lo fanno da 7 anni) con schede in cui si registrano progressi misurabili, effetti collaterali ecc. Di centinaia di pazienti trattati dicono a voce che il 70% sono guariti, ma non mostrano un dato. Perché non li hanno raccolti, per loro stessa ammissione. Dicono che il sistema è sicuro, ma si sa per certo che un paziente ha avuto una crisi epilettica (Vannoni dice che era una conseguenza della malattia di base, ma potrebbe dire anche che era colpa di quel che ha mangiato a cena… non c’è alcuna prova clinica di quel che dice), la bimba Nicole ha avuto nausea e cefalea gravi, tanto da finire in PS, subito dopo un’ iniezione (questo è sicuramente causato dall’ iniezione, in quanto notoriamente si può verificare dopo una puntura lombare; non dico che sia causato dalle staminali, ma dal modo con cui sono state somministrate), un altro bambino immediatamente dopo l’iniezione ha avuto una crisi respiratoria per cui è stato rianimato (questo è scritto in una lettera di dimissione mostrata dalle Iene!). Tre episodi che possono essere casuali o no, (guardi questo link, http://medbunker.blogspot.it/2013/11/stamina-e-guarigioni-la-salute-ai-tempi.html
in particolare seconda e terza immagine). E i risultati che mostrano sono solo su bambini con patologie in cui non è possibile misurare i progressi ma solo basarsi su impressioni (i muscoli più morbidi, una maggior reattività agli stimoli, regge il capo per qualche secondo…). E ogni volta che salta fuori qualcuno che non ha avuto progressi, la colpa è sempre di qualcosa’ altro: le cellule venivano da un laboratorio diverso, avevano sospeso le infusioni (un bambino è morto un mese dopo l’iniezione, uno 45 giorni dopo), i genitori mentono, i medici curanti mentono… Cioè: se il paziente migliora è merito delle cellule staminali, se non migliora o sta male è colpa della malattia di base, del laboratorio, del viaggio, del caso… troppo comodo!
4) è evidente che lei non capisce niente di sperimentazione clinica, legge qua e là articoli di cui non capisce niente e di cui coglie solo quello che supporta la tua tesi preconcetta. Ma si faccia una semplice domanda: PERCHE’ MIGLIAIA DI RICERCATORI IN TUTTO IL MONDO SPRECANO TEMPO E SOLDI A SPERIMENTARE UN PASSO ALLA VOLTA? SONO TUTTI SCEMI E AUTOLESIONISTI? O NON E’ INVECE VANNONI CHE SFUGGE A QUESTO SISTEMA PERCHE’ HA LA CODA DI PAGLIA?
5) Le sembra che “uno dei meriti di Vannoni e di non aver sprecato soldi e tempo con animali.” Cerro, i soldi non li ha sprecati LUI, ma lo stato italiano che ha speso 1.000.000 di euro per trattare dei pazienti senza avere uno straccio di documentazione che illustri onestamente quanti sono migliorati, quanti invariati, quanti peggiorati e quanti effetti collaterali sono stati osservati?
http://www.wired.it/scienza/medicina/2014/01/22/stamina-indagini-spreco-denaro-pubblico/
questi non sono certo concorrenti prezzolati da case farmaceutiche.
http://www.corriere.it/salute/14_gennaio_25/stamina-l-ospedale-che-mise-vannoni-porta-non-sapeva-nulla-cellule-staminali-f81ffa5a-8591-11e3-97a7-e7402e9bb91d.shtml
in questo momento i giornali mi sembrano poco oggettivi, anzi..ultimamente su staminal e sulla sa mi sembrano vere e proprie campagne propagandistiche..anzi, se devo dirla tutta, ho questo sentore da lustri…per questo preferisco i documenti..infatti mi chiedo, i documenti che hanno mostrato le Iene qualche giorno fa per voi sono quadri astratti??
p.s. ho copiato e incollato TUTTO proprio per evitare i timori che ha esplicitato nel suo commento.
I documenti che hanno poresentato le Iene sono abili mistificazioni, in cui si mostra solo quello che si vuole mostrare e si nasconde quello che contrasta la teoria:
http://medbunker.blogspot.it/2013/11/stamina-e-guarigioni-la-salute-ai-tempi.html http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3840989/pdf/ijsc-05-73.pdf
mentre lo setsso Andolina a suo tempo ha detto che le sue infusioni non rigeneravano un bel nulla, visto che in 30 giorni scopmariva l’effetoo! i
[…] neuronale. Poi abbiamo il rapporto dei NAS e il testo dell’ordinanza dell’AIFA, stralci di analisi effettuate dal laboratorio degli Spedali Civili di Brescia, qualche dato pubblicato su Facebook, […]
I’ve been absent for a while, but now I remember why I used to love this website. Thanks, I’ll try and check back more frequently. How frequently you update your site? eeceddedfk
[…] l’Intruglio Stamina). Quei famosi marker molecolari di cui si è parlato tempo fa, infatti, non bastano. Per essere una Ferrari non è sufficiente avere quattro ruote ed essere dipinti di rosso: bisogna […]