La chimica è una materia che sbalordisce sempre. Infatti oggi parleremo di una materiale dalle proprietà sorprendenti: il grafene.
Negli ultimi decenni, il grafene si è affermato come uno dei materiali più promettenti nella scienza dei materiali. In questo articolo, esploreremo la rivoluzione di questo composto e di come stia cambiando il mondo.
COSA SI INTENDE PER CHIMICA DEL CARBONIO?
In chimica è fondamentale conoscere la struttura nello spazio di un composto, perché da essa possiamo avere delle importanti informazioni riguardanti la sua funzione e le caratteristiche macroscopiche.
Interessante soprattutto dal punto di vista strutturale è il carbonio.
Che cos’è il carbonio? E’ un elemento chimico con simbolo C, numero atomico 6, peso atomico 12,01, di cui sono noti in natura gli isotopi stabili 12C, 13C (che ne costituiscono rispettivamente il 98,892% e l’1,108%), e 14C radioattivo (che si forma nell’atmosfera in conseguenza di reazioni nucleari tra l’azoto atmosferico e i neutroni lenti della componente secondaria dei raggi cosmici).
Il carbonio è un elemento chimico che può formare diverse forme allotropiche.
COSA SI INTENDE PER ALLOTROPIA?
In chimica, l’allotropia si riferisce alla capacità di un elemento di esistere in diverse forme strutturali o fisiche, chiamate forme allotropiche, in cui gli atomi dello stesso elemento sono disposti in modo diverso. Queste diverse forme allotropiche possono avere proprietà fisiche e chimiche significativamente diverse.
L’allotropia si verifica quando gli atomi di un elemento si combinano tra loro in modi diversi per formare strutture cristalline o molecole con legami chimici differenti. Queste diverse configurazioni atomiche conducono a differenze nelle proprietà delle forme allotropiche dell’elemento, come punto di fusione, punto di ebollizione, durezza, conduttività elettrica, reattività chimica e altre caratteristiche fisiche.
Il carbonio è un esempio noto, perché esiste in diverse forme allotropiche, tutte con caratteristiche peculiari.
Le più note forme di allotropi del carbonio sono: la grafite, il diamante, i fullereni e i nanotubi di carbonio.
La grafite è una forma comune di carbonio, costituita da strati di atomi di carbonio disposti in un reticolo esagonale. I legami tra gli atomi di carbonio in ciascuno strato sono forti, mentre i diversi strati sono tenuti insieme tra di loro tramite forze di Van der Waals (interazione di natura debole). La grafite è utilizzata in matite, lubrificanti e in diverse applicazioni industriali.
Il diamante è una delle forme più conosciute del carbonio. La differenza tra grafite e diamante è stata già trattata da pillole di chimica in un articolo dal titolo: “un diamante è per sempre?”
Esso infatti è caratterizzato da una struttura cristallina tridimensionale, in cui ciascun atomo di carbonio è legato a quattro atomi di carbonio adiacenti tramite legami covalenti tetraedrici. Questa struttura conferisce al diamante la sua durezza eccezionale, rendendolo una delle sostanze più dure conosciute. Il diamante è ampiamente utilizzato come gemma preziosa e in applicazioni industriali, come punte di trapano e utensili di taglio.
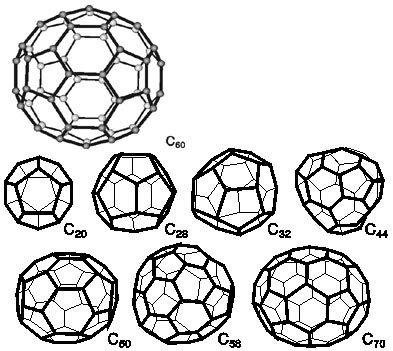
I fullereni invece sono molecole di carbonio costituite da strutture sferiche o tubulari. Le molecole di fullerene, costituite interamente di carbonio, assumono una forma simile a una sfera cava, a un ellissoide o a un tubolare. I fullereni di forma simile a una sfera o a un ellissoide sono chiamati buckyball, mentre quelli di forma tubolare sono chiamati buckytube o nanotubi di carbonio.
La differenza principale con il grafene è che la loro struttura esagonale planare è intervallata da quella pentagonale che impedisce una struttura planare.
Il fullerene C60, noto come buckminsterfullerene, che ha una forma sferica composta da 60 atomi di carbonio disposti come pentagoni ed esagoni, è stato scoperto nel 1985 e ad oggi sono numerosi gli studiosi che si occupano di questi composti per comprendere le loro possibili applicazioni future.
I nanotubi di carbonio sono strutture cilindriche costituite da un singolo strato o da più strati di grafene arrotolati. Questi nanotubi possono avere proprietà elettriche, termiche e meccaniche straordinarie e hanno una vasta gamma di applicazioni, come materiali compositi, dispositivi elettronici e filtri.
CHE COS’È IL GRAFENE E A COSA SERVE?
E arriviamo al nostro grafene. Il grafene è una forma bidimensionale di carbonio composta da un singolo strato di atomi di carbonio disposti in una struttura esagonale. Ha proprietà uniche, come eccellente conducibilità elettrica e termica, alta resistenza e flessibilità. Il grafene è ampiamente studiato per le sue potenziali applicazioni in elettronica, materiali compositi, energia e altro ancora. Ma cerchiamo di capire la chimica dietro a queste fantastiche proprietà.
Ogni atomo di carbonio nel grafene è ibridato sp2, il che significa che tre dei suoi elettroni di valenza partecipano alla formazione di legami covalenti con altri atomi di carbonio. Questi legami sono noti come legami σ (sigma) e ogni atomo di carbonio forma tre di questi legami, formando una struttura a esagono. Questi legami sono molto forti e conferiscono al grafene la sua notevole resistenza meccanica.
La struttura del grafene è caratterizzata anche dalla presenza di un legame π (pi) che si estende sopra e sotto il piano degli atomi di carbonio. Questo legame π è responsabile delle proprietà elettroniche uniche del grafene, come la sua eccellente conducibilità elettrica.
Struttura ulteriormente convalidata anche nel 2009 da un gruppo di ricercatori dell’IBM di Zurigo, i quali hanno realizzato immagini così dettagliate di una molecola da riuscire a determinare anche il tipo di legame tra gli atomi che la compongono.

Una molecola di grafene , composto esclusivamente da atomi di carbonio fotografato grazie al microscopio a forza atomica. Foto: © IBM Research – Zurich
Quindi immaginate di avere un “lenzuolo” esagonale di atomi di carbonio, molto flessibile ma anche resistente, che potete stendere in lungo e largo; soprattutto ogni singolo foglio è spesso quanto un solo atomo. Per questo si parla di grafene come di un materiale bidimensionale, in cui esistono solo le due dimensioni del piano.
DOVE TROVO IL GRAFENE?
Tutti voi conoscete le mine della matite. Ecco queste mine sono essenzialmente formate da grafite. Come abbiamo detto precedentemente la grafite è costituita da strati di atomi di carbonio disposti in un reticolo esagonale. Immaginate che la grafite sia un libro formato da pagine una sopra l’altra di grafene. Ecco se riuscissimo a separare queste “pagine esagonali” otterremmo il grafene.
Quindi il grafene può essere prodotto in laboratorio utilizzando diverse tecniche di sintesi, sia con metodi chimici che fisici.
COME È STATO SCOPERTO IL GRAFENE?
Come spesso succede in ambito scientifico l’affermazione Eureka viene sostituita da “ma che strano!” Ed è il caso dei due scienziati russi, Andrej Gejm e il suo studente Konstantin Novosëlov, che nel 2004 a Manchester cercavano di ottenere delle strutture molto sottili di grafite. Per assottigliare sempre più delle scaglie di grafite, Gejm e Novosëlov provarono a usare del nastro adesivo, sì avete capito bene un banalissimo nastro adesivo!

Gli scienziati che hanno scoperto il grafene: Andrej Gejm e Konstantin Novosëlov- Di Sergeom – Opera propria, CC0, Di Zp2010 – Opera propria, CC BY-SA 3.0
Strappando via di volta in volta strati di grafite, riuscirono ad ottenere invece un singolo strato monoatomico: appunto il grafene.
Successivamente Andrej Gejm spiegò l’importanza della scoperta, che nel 2010 lì permise insieme al suo collega di vincere il premio Nobel per la fisica. In teoria, uno strato monoatomico di un qualsiasi materiale non potrebbe esistere. «Il motivo è che viviamo in un mondo 3D», spiega lo scienziato russo, «quindi le strutture 2D come il grafene non potrebbero formarsi: tenderebbero a distorcersi per creare strutture 3D, come la grafite, i fullereni e i nanotubi. Però noi abbiamo creato il grafene in modo diverso: lo abbiamo ottenuto dalla grafite».
PROPRIETÀ E APPLICAZIONI FUTURE DEL GRAFENE.
Sul grafene potremmo parlare e scrivere interi libri, ma prima di addormentarvi con una lettura soporifera cercherò di elencarli e spiegarli in modo più semplice possibile. Intanto partiamo con il dire che questo materiale è molto resistente: nonostante la sue struttura bidimensionale atomica, il grafene è circa 200 volte più resistente dell’acciaio, ma allo stesso tempo leggero e flessibile. Queste sue caratteristiche meccaniche lo rendono un candidato formidabile come materiale per rivestimenti di ultima generazione. Questo può avere applicazioni nel settore aerospaziale o automobilistico, ma non solo…
Inoltre non tutti lo sanno, ma il grafene è uno dei materiali più conduttivi che si conoscano. La sua capacità di trasportare elettroni ad alta velocità lo rende promettente per applicazioni nell’elettronica ad alta frequenza, nell’elettronica flessibile e nei dispositivi di nuova generazione. Queste caratteristiche lo rendono ottimo non solo per batterie al grafene ma anche per la realizzazione di supercondensatori, in grado di immagazzinare più energia e di ricaricarsi più in fretta.
Ha anche un’elevata conducibilità termica, capacità che gli consente un eventuale uso anche per celle solari ad alta efficienza.
E parlando di proprietà ottiche, il grafene assorbe solo il 2,3% della luce visibile e ha una capacità di assorbimento dei fotoni molto elevata.
Questo materiale ha dimostrato un potenziale significativo nell’applicazione come materiale per la desalinizzazione dell’acqua, un processo che rimuove il sale e altre impurità dall’acqua di mare o salmastra per renderla potabile o adatta per usi agricoli o industriali.
Quindi le membrane a base di grafene possono consentire il passaggio selettivo dell’acqua attraverso di esse. E questo è molto importante per affrontare le sfide dell’approvvigionamento di acqua dolce nelle regioni con scarsità di risorse idriche.
Ultimo, ma sicuramente non per importanza, è il potenziale che il grafene potrebbe avere in campo medico.
Sono numerosi gli studi in atto in campo dei biosensori: potrebbe essere utilizzato per sviluppare biosensori altamente sensibili per la rilevazione di biomolecole e indicatori biologici. Come abbiamo già detto, le sue proprietà ottiche e di assorbimento dei fotoni possono essere sfruttate per migliorare la qualità e l’accuratezza delle immagini ottenute tramite tecniche come la risonanza magnetica (MRI) e la tomografia a emissione di positroni (PET).
Grazie alle sue proprietà di conducibilità elettrica, flessibilità e biocompatibilità, il grafene può migliorare l’interfaccia tra i dispositivi e il tessuto biologico o persino può essere utilizzato nell’ingegneria dei tessuti per la rigenerazione e la riparazione di tessuti danneggiati o per la creazione di strutture tridimensionali che simulano l’ambiente dei tessuti umani.
Ovviamente tutte queste applicazioni sono ancora in fase di ricerca e studio approfondito e richiederanno ulteriori test per valutare la loro efficacia, sicurezza e possibilità di traduzione in applicazioni cliniche. “Eppur si muove” qualcosa in questo settore!
Insomma, la rivoluzione del grafene è iniziata e il suo impatto potenziale sul nostro mondo è stupefacente. Le sue proprietà uniche e straordinarie stanno spingendo avanti l’innovazione in molti settori, aprendo la strada a nuove tecnologie e applicazioni mai immaginate in precedenza. Incrociamo le dita e continuiamo con la ricerca.
FONTI:
- Novoselov, K. S., & Geim, A. K. (2007). The rise of graphene. Nature Materials, 6(3), 183-191.
- Geim, A. K., & Novoselov, K. S. (2010). The rise of graphene. Physics Today, 63(11), 35-41.
- Cantele, Y.S. Lee, N. Domenico e N. Marzari, Spin Channels in Functionalized Graphene Nanoribbon,. Nano Letters Vol. 9, No. 10, 2009 3429
- Castro Neto, A. H., Guinea, F., Peres, N. M. R., Novoselov, K. S., & Geim, A. K. (2009). The electronic properties of graphene. Reviews of Modern Physics, 81(1), 109-162.
- Raccichini, R., Varzi, A., Passerini, S., & Scrosati, B. (2015). The role of graphene for electrochemical energy storage. Nature Materials, 14(3), 271-279.
- Wang, X., Zhi, L., & Müllen, K. (2008). Transparent, conductive graphene electrodes for dye-sensitized solar cells. Nano Letters, 8(1), 323-327.
- https://www.geopop.it/grafene-cose-quali-sono-le-sue-proprieta-e-le-sue-applicazioni/
- https://grafene.cnr.it/il-grafene-proprieta-e-applicazioni/
- https://www.focus.it/tecnologia/innovazione/a-18-anni-inventa-il-modo-per-depurare-lacqua-con-il-grafene












Scrivi un commento